熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
摘要:
膿毒癥誘發(fā)的肝功能障礙被認(rèn)為是多器官功能障礙綜合征(MODS)和死亡的獨立風(fēng)險因素。有絲分裂是自噬的一種選擇性形式,在膿毒癥誘發(fā)的器官損傷中發(fā)揮著重要作用。我們已經(jīng)證明,氫氣(H2)是一種選擇性抗氧化劑,對膿毒癥小鼠有保護作用。在此,我們假設(shè)氫氣對膿毒癥動物肝臟損傷的治療作用可能是通過調(diào)節(jié)Fun14含域蛋白1(FUDNC1)誘導(dǎo)的有絲分裂途徑實現(xiàn)的。雄性C57BL/6J小鼠接受假手術(shù)或盲腸結(jié)扎術(shù)(CLP),并在假手術(shù)或CLP手術(shù)后1小時開始吸入2%的H2氣體治療3小時。為了驗證FUNDC1的作用,在假手術(shù)或CLP手術(shù)前24小時,向小鼠腹腔注射了具有FUNDC1抑制作用的細(xì)胞穿透肽P(1mg/kg)。為了評估膿毒性肝損傷的嚴(yán)重程度,我們評估了假手術(shù)或CLP手術(shù)后的7天存活率、肝組織病理學(xué)評分、丙氨酸氨基轉(zhuǎn)移酶(ALT)和天冬氨酸氨基轉(zhuǎn)移酶(AST)水平、呼吸控制比(RCR)以及FUDNC1、P-18-FUDNC1、P62、LC3B-II、Tim23和caspase-1水平。結(jié)果表明,吸入2%H2氣體可提高敗血癥后的7天存活率、ALT和AST水平、RCR、P62和LC3B-II表達,但會降低組織學(xué)評分以及FUDNC1、P-18-FUDNC1、Tim23和caspase-1水平。然而,CLP+肽P組和CLP+H2+肽P組之間沒有明顯差異。這些觀察結(jié)果表明,吸入2%H2氣體3小時可通過調(diào)節(jié)FUNDC1依賴性的有絲分裂,作為膿毒癥誘導(dǎo)的肝損傷的有效治療策略。
引言:
敗血癥是由入侵微生物誘發(fā)的一種公認(rèn)的全身炎癥反應(yīng)綜合征(SIRS)。敗血癥的發(fā)病率已從1.5%上升到8%,全球每年有超過1800萬人罹患敗血癥。然而,目前還沒有治療敗血癥的有效方法。作為人類最大的腺體,肝臟在膿毒癥的新陳代謝和免疫平衡中發(fā)揮著關(guān)鍵作用。在敗血癥期間,入侵的細(xì)菌及其產(chǎn)物首先被肝細(xì)胞捕獲并清除。與此同時,肝臟免疫細(xì)胞釋放促炎介質(zhì),可能導(dǎo)致急性肝損傷。有證據(jù)表明,急性肝功能不全和衰竭可能直接導(dǎo)致敗血癥患者病情惡化和死亡,而改善肝損傷或恢復(fù)肝功能可降低這些患者的發(fā)病率和死亡率。
分子氫(H2)是一種特殊的選擇性抗氧化劑,可有效用于治療70多種疾病。與維生素E等傳統(tǒng)抗氧化劑相比,氫具有兩個獨特的特性。首先,它能輕易穿透細(xì)胞膜,迅速轉(zhuǎn)移到細(xì)胞核和線粒體。其次,它能選擇性地中和細(xì)胞毒性較強的羥基(OH-)和過氧亞硝酸(ONOO-)自由基,而不與毒性較弱的活性氧(ROS)發(fā)生反應(yīng)。我們之前的研究表明,吸入H2氣體或飲用富含氫氣的生理鹽水可有效防止敗血癥和敗血癥引起的器官損傷,包括肝、肺、腦和腎。我們還展示了吸入2%H2氣體可顯著緩解肝損傷,提高敗血癥小鼠的7天存活率。然而,其根本機制仍不清楚。
線粒體為有機生命提供約90%的能量,是細(xì)胞的重要組成部分。線粒體還具有多種其他生物功能,包括調(diào)節(jié)ROS生成、細(xì)胞氧化還原反應(yīng)、信號轉(zhuǎn)導(dǎo)網(wǎng)絡(luò)和細(xì)胞凋亡。在敗血癥患者中,重要器官的線粒體功能障礙可能會降低細(xì)胞能量水平,導(dǎo)致多器官功能衰竭。臨床研究表明,針對線粒體功能障礙的治療,而不是直接抑制炎癥級聯(lián)反應(yīng),可能會改善膿毒癥患者的預(yù)后。
作為自噬的一種選擇性形式,線粒體吞噬是在細(xì)胞器水平控制線粒體質(zhì)量的基本過程。線粒體網(wǎng)絡(luò)的維持和細(xì)胞新陳代謝的重編程也離不開絲裂噬。含F(xiàn)un14結(jié)構(gòu)域的蛋白1(FUNDC1)是絲裂噬受體之一,定位于線粒體外膜,在線粒體應(yīng)激和缺氧時參與清除受損的線粒體。FUNDC1可與LC3B-II相互作用,并通過一些關(guān)鍵位點的可逆磷酸化調(diào)控缺氧誘導(dǎo)的選擇性有絲分裂。
在此,我們旨在揭示FUNDC1誘導(dǎo)的有絲分裂在敗血癥引起肝損傷的發(fā)病機制中的作用,以及在敗血癥小鼠盲腸結(jié)扎和穿刺(CLP)模型中吸入2%H2氣體的保護機制。
材料與方法:
動物和實驗方案:
動物實驗方案須經(jīng)天津醫(yī)科大學(xué)總醫(yī)院機構(gòu)動物護理和使用委員會批準(zhǔn)。成年雄性C57BL/6J小鼠(6周齡,體重20-25g)來自軍事醫(yī)學(xué)科學(xué)院實驗動物中心。所有動物均在穩(wěn)定的環(huán)境(溫度22°C±1°C,濕度50%-60%,12:12h光暗循環(huán))中獲得充足的食物和水。小鼠隨機分為五組:假組、CLP組、CLP+肽P組、CLP+H2組和CLP+H2+肽P組。為了驗證FUNDC1的作用,在CLP或假手術(shù)前24小時給小鼠腹腔注射細(xì)胞穿透肽P,這是一種FUNDC1抑制劑。其他組小鼠注射相同體積的生理鹽水。膿毒癥模型由CLP產(chǎn)生。與CLP組小鼠相比,假手術(shù)組小鼠除CLP處理外,其余過程相同。CLP+H2組和CLP+H2+肽P組小鼠在假手術(shù)或CLP手術(shù)后1小時開始吸入H2氣體(2%)3小時,而假手術(shù)組、CLP組和CLP+肽P組小鼠僅吸入空氣(21%O2)。在假手術(shù)或CLP手術(shù)后1小時,分別在開始吸入H2氣體后的0、10、20、30、45、60、120和180分鐘,以及終止吸入H2氣體后的5、15、30、45和60分鐘測量各組小鼠動脈血和靜脈血中的H2氣體濃度。分析了假手術(shù)或中電刀手術(shù)后第1至7天各組的存活率。手術(shù)后6小時,我們處死小鼠并獲取血液樣本和肝組織。肝臟切片用于組織學(xué)檢查。從手術(shù)后6小時的肝組織中分離線粒體,分析呼吸控制比(RCR)。血液樣本中的丙氨酸氨基轉(zhuǎn)移酶(ALT)和天冬氨酸氨基轉(zhuǎn)移酶(AST)水平通過酶聯(lián)免疫吸附試驗(ELISA)測定,肝組織中的FUNDC1、p-18-FUNDC1、P62、LC3B-II和caspase-1水平通過Western印跡法測定(圖1)。
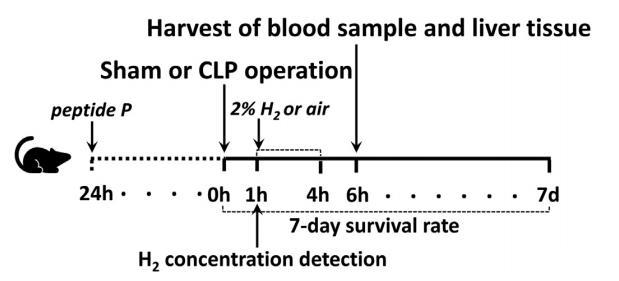
圖1:實驗設(shè)計。雄性C57BL/6J小鼠(6-8周大,體重20-25g)接受假手術(shù)或CLP手術(shù)。我們使用2%的氫氣(H2)或新鮮空氣處理小鼠,從假性或CLP手術(shù)后1小時開始,持續(xù)3小時。為了驗證FUNDC1的關(guān)鍵作用,我們在CLP或假手術(shù)前24小時給小鼠腹腔注射細(xì)胞穿透肽P(一種FUNDC1抑制劑);其他組則注射相同體積的生理鹽水。在假手術(shù)或CLP手術(shù)后6小時收集各組小鼠的血清樣本和肝組織。
CLP模型:
CLP模型的制作方法與我們之前的研究相同。首先,向小鼠腹腔注射溶于生理鹽水的2%戊巴比妥鈉作為麻醉。將小鼠放在特制的動物用無菌手術(shù)臺上,在腹部做一個長約1厘米的中線切口,暴露盲腸。結(jié)扎盲腸遠(yuǎn)端四分之一處,用20號針頭穿刺盲腸遠(yuǎn)端。通過穿刺點擠出部分排泄物。最后,將盲腸輕輕放回腹部,用無菌3-0號絲線縫合切口。手術(shù)后,向小鼠皮下注射1毫升生理鹽水進行復(fù)蘇。
H2氣體處理:
H2氣體處理程序按照之前的描述進行了一些修改。小鼠被放入一個密封的有機玻璃箱中,箱內(nèi)有進氣閥和出氣閥。由TF-1氣體流量計以4升/分鐘的速度向箱內(nèi)輸送與新鮮空氣混合的H2氣體。小鼠呼出的二氧化碳由一袋巴里梅清除。用一個特殊的手持探測器監(jiān)測H2氣體濃度。我們使用2%的H2氣體對小鼠進行治療,從術(shù)后1小時開始,持續(xù)3小時;而假小鼠或CLP組的小鼠則被放置在同一箱中,箱內(nèi)有空氣(21%O2),但沒有2%的H2氣體。
測量H2氣體濃度:
按照之前的描述,使用針式氫氣電極(UnisenseA/S,丹麥奧胡斯)檢測動物動脈和靜脈血樣本中的H2氣體濃度。在開始吸入H2氣體后的0、10、20、30、45、60、120和180分鐘以及結(jié)束吸入H2氣體后的5、15、30、45和60分鐘采集動脈和靜脈血樣本。
存活率測定:
觀察假手術(shù)或CLP手術(shù)后第1-7天的小鼠存活率。試驗重復(fù)兩次。
組織學(xué)分析:
在術(shù)后6小時獲得肝組織標(biāo)本(5μm),并用蘇木精-伊紅染色以評估肝損傷程度。用光學(xué)顯微鏡觀察肝損傷,評分標(biāo)準(zhǔn)如下:囊炎、門脈炎、斑點狀壞死、氣球變性和脂肪變性。
轉(zhuǎn)氨酶分析:
手術(shù)后6小時從小鼠左心室采集血樣,并使用自動生化分析儀檢測血清AST和ALT水平。
肝線粒體的分離:
肝臟線粒體通過傳統(tǒng)的差速離心法獲得。簡而言之,采集肝臟右葉并在冰冷的分離緩沖液中切碎,該緩沖液含有70mM蔗糖、220mM甘露醇、5mM HEPES、1mM苯甲磺酰氟(PMSF)和0.2%脫脂牛血清白蛋白(BSA),pH值為7.4。在分離培養(yǎng)基中用玻璃勻漿器將無血組織勻漿,勻漿在1500×g和4°C下離心10分鐘。上清液在12,000×g和4°C下離心10分鐘。排除上清液后,將線粒體顆粒重懸于含有70mM蔗糖、220mM甘露醇和5mM HEPES的培養(yǎng)基中。以BSA為標(biāo)準(zhǔn),采用Coomassie亮藍法測定線粒體蛋白水平。在線粒體呼吸測定過程中,將新獲得的線粒體懸浮液置于冰上(0-4°C)培養(yǎng),在4小時內(nèi)進行測定。
線粒體呼吸分析:
使用OroborosOxygraph-2K儀器在25°C下檢測線粒體呼吸。將肝臟線粒體加入反應(yīng)介質(zhì)中。將線粒體引入室中約5分鐘后,加入琥珀酸(5mM)。在觀察到穩(wěn)態(tài)4呼吸階段后,加入50mM ADP以達到狀態(tài)3呼吸狀態(tài)。總ADP的消耗將導(dǎo)致恢復(fù)到穩(wěn)態(tài)4呼吸階段。在兩次實驗之間,用清水和乙醇對實驗箱進行兩次清洗。根據(jù)狀態(tài)3/狀態(tài)4呼吸的比率計算RCR。
Western印跡分析:
手術(shù)后6h處死小鼠,收集不同組的肝組織,用放射免疫沉淀法(RIPA)緩沖液裂解提取蛋白質(zhì)。使用雙喹啉酸蛋白質(zhì)測定試劑盒對蛋白質(zhì)總量進行定量。等量用于檢測FUNDC1、p-18-FUNDC1、P62、LC3B-II和caspase-1的表達。一抗包括抗FUNDC1、抗p-18-FUNDC1、抗P62、抗LC3B-II多克隆、抗caspase-1:使用抗甘油醛-3-磷酸脫氫酶和特異性二抗。蛋白條帶用化學(xué)發(fā)光加試劑處理,并用增強化學(xué)發(fā)光(ECL)試劑顯色。使用GeneTools軟件計算各條帶的強度。FUNDC1、p-18-FUNDC1、P62、LC3B-II和caspase-1的相對水平與GAPDH水平進行歸一化。
統(tǒng)計分析:
存活率以百分比(%)表示,其他數(shù)據(jù)以均數(shù)±標(biāo)準(zhǔn)差(SD)表示。采用對數(shù)秩檢驗分析不同組的7天存活率。我們使用非配對t檢驗或Mann-Whitney檢驗來分析兩組(假組與中電組、中電組與中電+H2組、中電+肽P組與中電+H2+肽P組)之間的差異。我們還使用單因素方差分析(ANOVA)來分析所有組間的交互作用。P<0.05的值被認(rèn)為具有統(tǒng)計學(xué)意義。
FUNDC1依賴性線粒體自噬及氫氣電極驗證:氫氣緩解膿毒癥肝損傷的機制——引言、材料與方法
 相關(guān)新聞
相關(guān)新聞