熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
3.結果與討論
3.1通過US EPA測試方法驗證抗菌功效
測試培養(yǎng)物、中和劑溶液和載體均成功通過了根據(jù)US EPA測試方法程序指南進行的所有無菌性、存活率、定量和抗菌敏感性對照。測試微生物的初始濃度約為10?CFU mL?1(表1),符合US EPA關于銅合金表面作為消毒劑的功效(方案1)和持續(xù)減少細菌污染(方案2)的測試方法。金黃色葡萄球菌ATCC 6538和耐甲氧西林金黃色葡萄球菌(MRSA)ATCC 33592被銅銀合金涂層有效滅活,與不銹鋼對照載體相比,在2小時(方案1)和24小時間隔內(nèi)的所有時間點均減少了5個對數(shù),減少百分比大于99.9%(表1)。銅銀合金涂層表面在方案1和方案2中,除2小時后不銹鋼對照載體上的水平約為102CFU每載體外,在其他所有時間點也將產(chǎn)氣腸桿菌ATCC 13048的水平降低了5個對數(shù)。然而,與未涂層的不銹鋼表面相比,銅銀合金涂層在方案1和方案2中的減少百分比均大于99.9%(表1)。
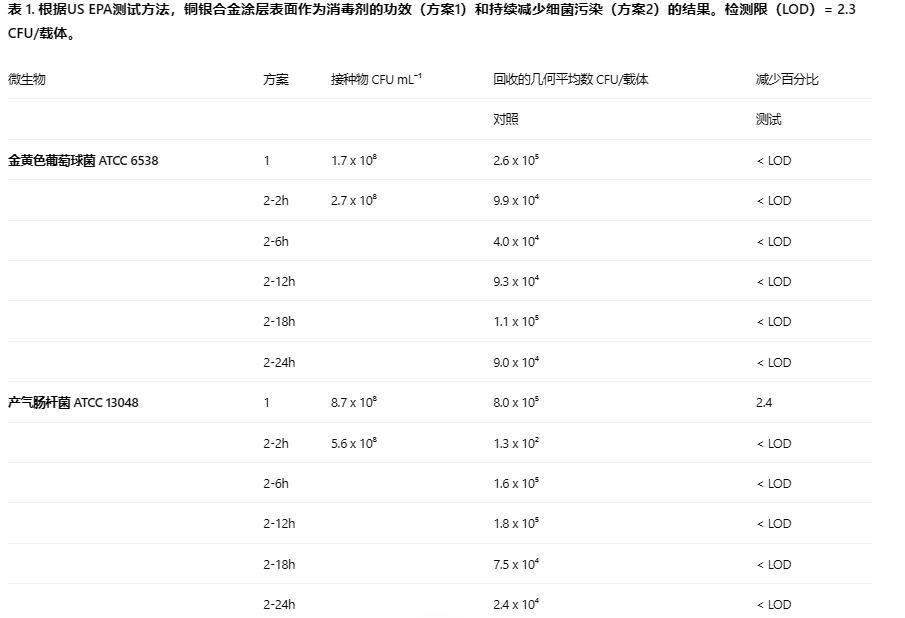
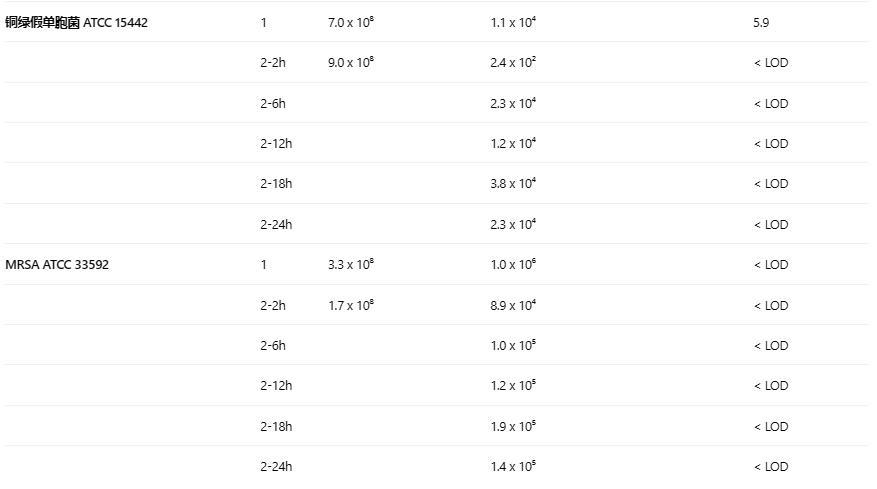
在方案1中,銅綠假單胞菌ATCC 15442能夠在銅銀合金涂層表面上存活,幾何平均數(shù)為每載體5.9 CFU,因此與不銹鋼對照表面(存活銅綠假單胞菌的幾何平均數(shù)為1.1 x 10?CFU每載體)相比,減少百分比為99.9%。然而,在方案2中,從2小時后的2個對數(shù)減少到6、12、18、24小時后的4個對數(shù)減少,減少百分比大于99.9%(表1)。因此,銅銀合金涂層表面成功通過了測試方法的驗收標準,即在暴露2小時后減少百分比≥99.9%,在24小時間隔內(nèi)的所有時間點減少百分比≥99.0%。
3.2共聚焦激光掃描顯微鏡(CLSM)和生物量定量
為了可視化暴露于銅表面后膜受損的細菌細胞,活/死染色技術和熒光顯微鏡是顯而易見的選擇,可以輕松區(qū)分具有完整(綠色熒光)和受損(紅色熒光)膜的細菌細胞。然而,觀察到常規(guī)熒光指示劑染料由于銅的光吸收特性,在與金屬銅表面接觸時會失去熒光。可以在染色前簡單地將細胞從表面移除然后檢查,但這只能允許在設定的暴露時間后對接觸殺滅造成的損傷效應進行事后可視化,而不能在銅表面進行原位跟蹤。


在此,使用改良的活/死染色程序和CLSM,在100分鐘的時間間隔內(nèi),將金黃色葡萄球菌8325(圖1)和銅綠假單胞菌PAO1(圖2)細胞暴露于銅銀合金涂層和未涂層的AISI 316樣品表面并直接觀察。在暴露于銅銀合金涂層表面的最初10分鐘內(nèi),金黃色葡萄球菌8325死細胞(紅色)的數(shù)量超過了活細胞(綠色)的數(shù)量(圖1和圖3)。25分鐘后,剩余的活細胞少于20%(圖3a),并且大多數(shù)細胞在60分鐘后呈現(xiàn)紅色(圖1d)。相比之下,暴露于AISI 316表面的金黃色葡萄球菌8325細胞保持存活(圖1e-h),并且其百分比在整個暴露期間大約保持在80%以上(圖3b)。暴露于銅銀合金涂層表面的銅綠假單胞菌PAO1活細胞數(shù)量從暴露開始到60分鐘隨時間減少(圖2a-d),此時活細胞和死細胞的比例轉向后者,死細胞數(shù)量開始增加(圖3c)。在AISI 316表面上,銅綠假單胞菌PAO1細胞保持存活(圖2e-h),并且其百分比在100分鐘的暴露期間接近100%(圖3d)。
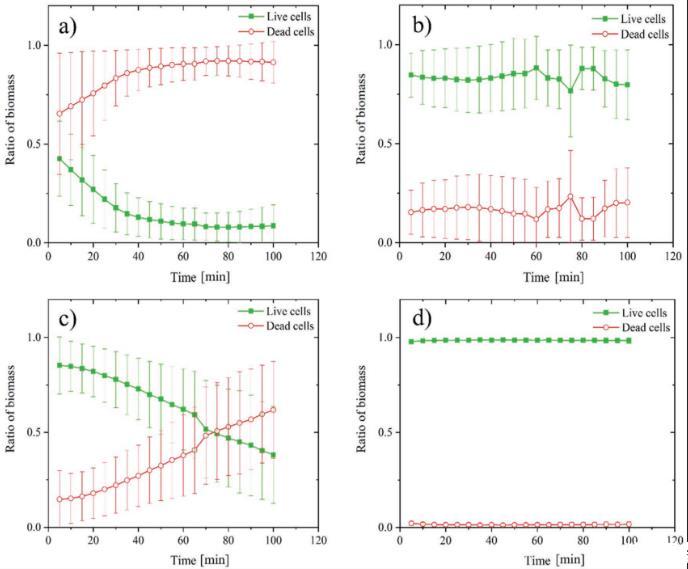
在金屬表面的直接觀察證實了銅銀合金涂層表面與未涂層不銹鋼對照相比的抗菌功效,正如在US EPA方案測試中也觀察到的那樣。銅銀合金涂層表面對金黃色葡萄球菌的殺滅速度比對銅綠假單胞菌更快,并且在US EPA作為消毒劑的功效測試方法(方案1)中也觀察到銅綠假單胞菌數(shù)量的減少百分比較低。使用US EPA測試方案測試的氧化銅浸漬非多孔固體表面,并未在所有測試中達到對銅綠假單胞菌99.9%的減少。因此,這些發(fā)現(xiàn)可能表明銅綠假單胞菌在一定程度上能夠抵抗暴露和接觸銅基表面。在接觸殺滅過程中,當銅因細菌膜的存在而從銅銀合金涂層表面溶解時,銅離子會在那個有限的空間內(nèi)積累。隨后發(fā)生膜損傷,銅離子進入細菌細胞質。革蘭氏陰性菌中存在被周質空間隔開的兩個細胞膜,以及可能在接觸殺滅抑制代謝活動之前存在的不同銅穩(wěn)態(tài)機制,可以解釋觀察到的銅綠假單胞菌殺滅延遲。然而,革蘭氏陽性和陰性細菌中的銅穩(wěn)態(tài)機制尚未完全闡明,并且在界面處檢測游離銅離子的濃度存在嚴重的實際問題。
3.3銅銀合金涂層和未涂層表面的pH監(jiān)測
在金黃色葡萄球菌8325懸浮液層與銅銀合金涂層表面之間的界面附近,pH以約0.14 pH單位/分鐘的速率增加,在20分鐘后達到pH 9.0以上的平臺期(圖4)。相比之下,在金黃色葡萄球菌8325懸浮液層與AISI 316表面之間的界面處,pH在10分鐘后從7.5-7.2之間的值下降到7.1-6.7之間的值,速率約為0.03 pH單位/分鐘。20分鐘后,pH達到7.0-6.5之間的平臺值(圖4)。這清楚地證明了銅銀合金涂層表面的電化學活性以及在水界面發(fā)生還原反應(O?+2H?O+4e?→4OH?)并產(chǎn)生OH?離子,從而局部升高pH。如果銅銀合金浸入含氯化物的環(huán)境中,則會建立電偶腐蝕條件。在0.15 M鹽水溶液中,銀和銅的腐蝕電位分別為120 mV和15 mV(相對于標準氫電極)。
因此,在電偶對中,較貴重的金屬銀以銅的消耗為代價受到保護,并且其溶解速率隨合金中銀含量的增加而增加。金黃色葡萄球菌在pH 5.0至7.0范圍內(nèi)的膜電位約為-100 mV(通過[3H]四苯基鏻TPP?的分布測量)。因此,在一個由兩種合金金屬和存在于0.15 M NaCl瓊脂糖基質中的金黃色葡萄球菌8325懸浮液組成的三元素系統(tǒng)中,也建立了一個電偶序列,其中銀具有最高的電化學電位,其次是銅和細菌物質。因此,有機物質容易氧化,因為它具有最低的電化學電位,而金屬合金則成為還原反應的場所。銅以其催化活性而聞名,這可能影響了反應速率,從而影響了OH?的產(chǎn)生速率。
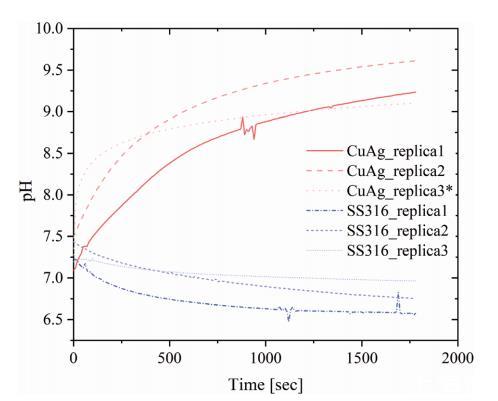
此外,細菌生物膜的存在阻止了氧化銅的形成,保持了合金涂層表面的活性,并為氧化還原反應以平衡速率進行提供了足夠的物質,如20分鐘后的平臺期所示(圖4)。相比之下,未涂層的不銹鋼只是一個惰性基底,pH的降低可能是未受挑戰(zhàn)的細菌懸浮液與0.15 M NaCl瓊脂糖基質接觸后調整至最佳pH條件的結果。如果金黃色葡萄球菌8325懸浮液不存在于瓊脂糖基質和銅銀合金涂層表面之間的界面處,pH會以0.69 pH單位/分鐘的速率從7.0-7.5之間的值(圖5,重復2和3)增加到4分鐘后的峰值9.5-10.0。在重復1的情況下(圖5),測量開始時的pH已經(jīng)是9.0,并在1分鐘后達到其峰值9.4。然后,pH開始以較慢的速率(約0.12 pH單位/分鐘)下降,在20分鐘后達到8.2-7.6之間的值。當在瓊脂糖基質和AISI 316表面之間的界面處監(jiān)測pH時,它在整個測量期間保持在大約6.4-6.7之間的恒定值(圖5)。
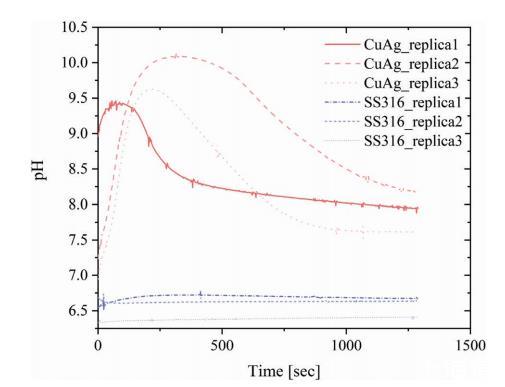
一旦0.15 M NaCl瓊脂糖基質與銅銀合金涂層表面之間的接觸建立,氧化還原反應立即開始。在這種雙金屬腐蝕條件下,銀位點上的還原反應產(chǎn)生了使pH升高的OH?,同時銅從合金涂層表面溶解。銅離子隨后與周圍環(huán)境反應形成氧化亞銅Cu?O。Cu?O的存在然后導致pH下降,因為在金屬表面建立了新的平衡條件。不銹鋼表面在沒有細菌懸浮液層的情況下也是一種電化學非活性基底,這從界面處測得的恒定pH值可以明顯看出。
3.4金黃色葡萄球菌8325暴露于pH 7.0至9.5的1 M Tris-HCl緩沖液
由于觀察到銅銀合金涂層表面pH的變化,我們質疑這種pH升高是否是快速接觸殺滅的主要原因。因此,我們將初始濃度約為10?CFU mL?1(對應于OD600 2.0)的金黃色葡萄球菌8325暴露于pH 8.0、8.5、9.0和9.5的1 M Tris-HCl緩沖液中,并在25°C下培養(yǎng)1小時和24小時。
暴露1小時后,金黃色葡萄球菌存活水平在10?到10?CFU mL?1之間,并且在24小時后細胞水平也保持在10?CFU mL?1以上(表2)。在不同pH下暴露1小時和24小時后的存活率沒有統(tǒng)計學顯著差異(P>0.01)。暴露24小時后的1個對數(shù)減少是由緩沖條件引起的,無法與US EPA測試中接觸殺滅在2小時后觀察到的4到5個對數(shù)減少相比。這表明金黃色葡萄球菌的存活率不受暴露于pH 8.0-9.5范圍的1 M Tris-HCl緩沖液的顯著影響。因此,銅銀合金涂層表面pH的升高不太可能是細菌減少的主要原因,而更可能在銅銀合金涂層表面的接觸介導殺滅中起次要作用。在環(huán)境條件下,并在界面處存在細菌生物膜時,合金中銅和銀的電偶耦合會誘導氧化還原反應。與合金接觸的細菌細胞會氧化,因為它們具有最低的電位,并且在金屬位點會發(fā)生還原反應,導致OH?產(chǎn)生和局部pH升高。
結論
在本研究中,我們證明了銅銀合金涂層在干燥和類真實生活條件下對細菌污染的抗菌特性。我們使用了US EPA關于作為消毒劑的功效和持續(xù)減少細菌污染的測試方法,以及通過CLSM進行直接可視化。該合金成功通過了兩個EPA測試方法的驗收標準,在暴露2小時后減少百分比等于(銅綠假單胞菌ATCC 15442)或大于99.9%,并且在24小時間隔內(nèi)的所有時間點減少百分比大于99.9%。
在銅銀合金涂層和未涂層表面接觸殺滅的原位監(jiān)測過程中,我們發(fā)現(xiàn)對金黃色葡萄球菌8325生物膜的殺滅速率高于銅綠假單胞菌PAO1。革蘭氏陽性活細胞在暴露的最初幾分鐘內(nèi)顯著減少,而革蘭氏陰性菌的活細胞和死細胞比例在暴露60分鐘后轉向后者。膜差異和不同的銅穩(wěn)態(tài)機制可以解釋銅綠假單胞菌PAO1生物膜殺滅速率較慢的原因。
銅銀合金涂層表面的pH測量和監(jiān)測顯示,當金黃色葡萄球菌8325懸浮液存在于表面和瓊脂糖鹽水基質之間的界面處時,pH快速升高并在20分鐘后達到pH 9.0的平臺期。在沒有細菌物質的情況下,pH迅速升高至約9.5,并由于Cu?O的形成而下降。在未涂層的對照AISI 316表面未檢測到pH升高,這是由于缺乏電化學活性。當金黃色葡萄球菌8325懸浮在不同pH(范圍8.0-9.5)的緩沖溶液中時,未觀察到數(shù)量顯著減少,表明pH不可能是觀察到的抗菌特性的唯一原因。因此,OH?的產(chǎn)生是銅銀合金涂層表面接觸介導殺滅現(xiàn)象的一個方面,而不是直接原因。在環(huán)境條件下并存在細菌污染時,合金中銅和銀的電偶耦合會誘導氧化還原反應:與合金接觸的細菌細胞氧化,以及在金屬位點發(fā)生還原,導致局部pH升高。在相同條件下,在未被細菌細胞占據(jù)的表面區(qū)域,還原反應發(fā)生在銀位點,氧化反應發(fā)生在銅位點,導致銅離子釋放。
我們得出結論,銅銀合金在干燥條件下是一種有效的抗菌劑,可對抗細菌污染。合金中金屬的電偶耦合引起的氧化還原反應可能在環(huán)境條件下誘導細菌細胞氧化、銅離子釋放和局部pH升高。這三個因素的結合是觀察到的該合金涂層抗菌功效的原因,并將確保其在醫(yī)療環(huán)境預期環(huán)境應用中的特性。對金屬電化學反應性的理解可用于生產(chǎn)其他氧化還原活性金屬的組合,或基于電偶對的活性系統(tǒng),根據(jù)特定環(huán)境和應用定制元素的選擇。
 相關新聞
相關新聞