熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
分級(jí)正常氧高碳酸血癥期間的pHbrain變化
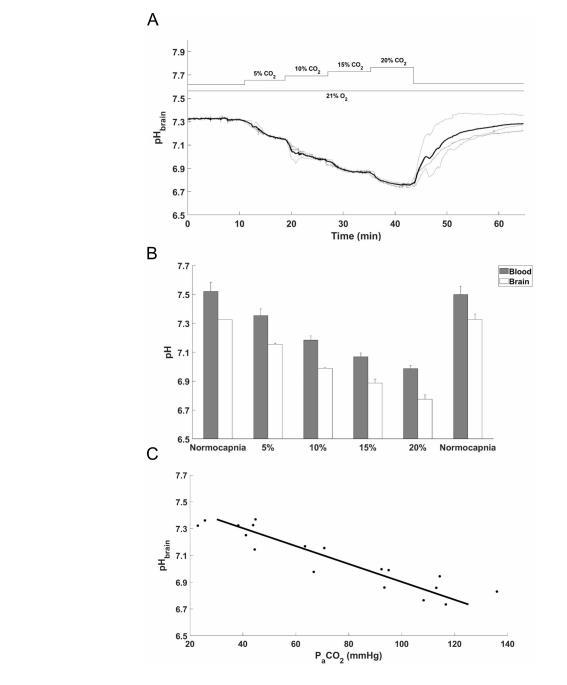
進(jìn)行這些實(shí)驗(yàn)是為了評(píng)估呼吸成分對(duì)PA期間記錄的pHbrain變化的貢獻(xiàn)。吸入CO?逐步增加5%(圖5A)導(dǎo)致pHbrain成比例地逐步降低(圖5B和5C)。動(dòng)脈血?dú)夥治鲲@示pHa類似的分級(jí)降低,因此在高碳酸血癥期間pHbrain和pHa之間的差異保持不變(圖5B)。在吸入20%CO?期間觀察到最大變化,此時(shí)pHa從7.52±0.06下降至6.98±0.02,而pHbrain從7.32±0.01下降至6.77±0.02。通過(guò)恢復(fù)正常碳酸血癥,pHbrain和pHa的變化完全逆轉(zhuǎn)。
討論
在本研究中,我們?cè)谝粋€(gè)轉(zhuǎn)化性仔豬PA/HIE模型中展示了PA期間和HIE亞急性期體內(nèi)實(shí)時(shí)記錄的pHbrain值。本研究的主要發(fā)現(xiàn)如下:(1)我們的實(shí)驗(yàn)?zāi)P鸵l(fā)了反映其主要特征的PA,并通過(guò)神經(jīng)病理學(xué)揭示了對(duì)應(yīng)于中度/重度HIE的神經(jīng)元損傷;(2)腦皮質(zhì)pHbrain對(duì)PA的反應(yīng)急劇下降,大腦中的酸中毒比動(dòng)脈血超過(guò)一個(gè)pH單位;(3)復(fù)蘇/再氧合使pHbrain恢復(fù)至基線水平,隨后pHbrain在基線水平附近保持穩(wěn)定,在24小時(shí)觀察期內(nèi)未發(fā)生重大偏移。
每個(gè)使用產(chǎn)后動(dòng)物的PA/HIE模型都不可避免地帶有局限性,即PA是在適應(yīng)宮外生活的心肺適應(yīng)之后而非之前/期間誘導(dǎo)的。然而,我們相信在本研究中,通過(guò)兩個(gè)因素將這種劣勢(shì)降至最低。首先,我們使用真正的新生豬,因此它們對(duì)PA的脆弱性不太可能因產(chǎn)后發(fā)育而發(fā)生顯著改變。其次,我們引發(fā)的PA導(dǎo)致了足夠嚴(yán)重的動(dòng)脈pH和血?dú)飧淖儯@些已知預(yù)示著人類HIE的發(fā)展。這一說(shuō)法有臨床研究支持,該研究報(bào)告了出現(xiàn)與未出現(xiàn)HIE的窒息嬰兒在酸中毒程度(pHa:6.75±0.18 vs 6.90±0.18)和高碳酸血癥程度(PaCO?:141±37 vs PaCO?:94±22 mmHg)上的顯著差異。在我們的模型中,相應(yīng)值為pHa:6.79±0.02和PaCO?:160±6 mmHg,與人類HIE患者組的數(shù)據(jù)非常接近。有趣的是,在分娩期間經(jīng)歷自發(fā)性PA的仔豬的臍動(dòng)脈血樣本中獲得了幾乎相同的值(pHa:6.69±0.04和PaCO?:156±4 mmHg),也表明仔豬作為PA/HIE模型物種的轉(zhuǎn)化價(jià)值。我們開發(fā)并使用該P(yáng)A/HIE方案來(lái)測(cè)試分子氫推定的神經(jīng)保護(hù)作用。我們?cè)诒狙芯恐袌?bào)告了與之前使用該P(yáng)A/HIE模型在窒息后24小時(shí)的新皮質(zhì)、海馬和皮質(zhì)下神經(jīng)元損傷幾乎相同。基于相似的神經(jīng)病理學(xué)發(fā)現(xiàn),我們可以假設(shè)與pHbrain測(cè)量相關(guān)的手術(shù)操作未影響本研究中HIE的發(fā)展,支持當(dāng)前pHbrain發(fā)現(xiàn)的轉(zhuǎn)化價(jià)值。
pHbrain在決定缺氧缺血應(yīng)激后神經(jīng)結(jié)局的重要性早已被認(rèn)識(shí)。然而,關(guān)于仔豬PA/HIE模型中/后pHbrain變化的定量數(shù)據(jù)在文獻(xiàn)中非常稀少。Bender等人使用類似技術(shù)評(píng)估了1-3日齡仔豬的pHbrain。PA也使用低氧高碳酸血癥氣體混合物(5-8%O?-7%CO?)誘導(dǎo)30分鐘。在PA結(jié)束時(shí),測(cè)得的pHbrain為6.26±0.14,比我們的研究高約0.3個(gè)pH單位,可能至少部分是由于PaCO?值低得多(61±1 vs.160±6 mmHg)。PA后,開始用100%O?通氣復(fù)蘇,此外,靜脈輸注碳酸氫鈉(2 mEq/kg)以快速糾正動(dòng)脈pH。Bender等人研究中的這兩種干預(yù)措施都可能降低其轉(zhuǎn)化價(jià)值,因?yàn)樗鼈兾窗诋?dāng)前的新生兒護(hù)理指南中,并且可能影響了pHbrain的恢復(fù),該恢復(fù)在90分鐘內(nèi)完成。此外,與假手術(shù)動(dòng)物相比,除PA與出血性低血壓結(jié)合的實(shí)驗(yàn)外,無(wú)顯著神經(jīng)元損傷,表明所應(yīng)用的PA本身嚴(yán)重程度不足以引發(fā)HIE。Corbett等人在8±3日齡仔豬中使用MRS測(cè)定缺血期間和之后的pHi,但非真正的PA。通過(guò)結(jié)合雙側(cè)頸動(dòng)脈閉塞和出血性低血壓25分鐘,隨后再灌注90分鐘,引發(fā)不完全性腦缺血。缺血期間發(fā)生嚴(yán)重酸中毒,其嚴(yán)重程度取決于應(yīng)激期間的血糖水平。在喂食仔豬中,腦pHi降至5.6以下,這些仔豬對(duì)缺血反應(yīng)為高血糖(9.4-15 mmol/L),而在禁食仔豬中,對(duì)缺血反應(yīng)為低血糖(1.4-2.6 mmol/L),缺血結(jié)束時(shí)的最低點(diǎn)僅為pHi≥6.6。再灌注后,pHi在90分鐘觀察期內(nèi)再次正常化。
從上述討論的研究可以清楚地看出,更高水平的高碳酸血癥、腦血流和血糖都會(huì)促進(jìn)PA期間腦酸中毒的發(fā)展。在人類和仔豬PA中觀察到的PaCO?升高至140-160 mmHg,單獨(dú)在正常氧條件下就會(huì)將pHi降低至6.5-6.6。同樣在本研究中,我們提供證據(jù)表明,在正常氧條件下,單獨(dú)吸入20%CO?(PaCO?:120 mmHg)會(huì)導(dǎo)致pHbrain下降至6.8。使用線性回歸(圖4C),我們計(jì)算出在我們PA模型中發(fā)展的高碳酸血癥(PaCO?:160 mmHg)單獨(dú)導(dǎo)致pHbrain下降至6.50,與之前的結(jié)果完全一致。PA期間的進(jìn)一步酸化將主要由無(wú)氧糖酵解速率增加推動(dòng)隨后的乳酸產(chǎn)生所決定。
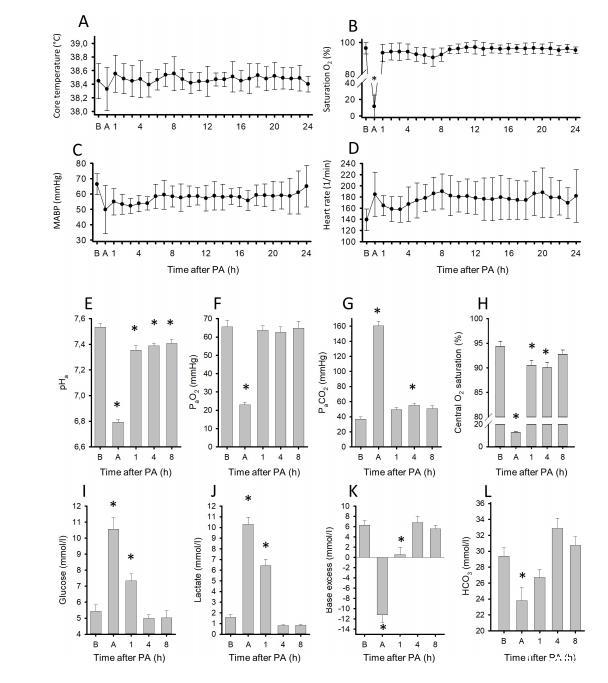
糖酵解速率受葡萄糖向缺氧大腦輸送的限制,因?yàn)橥ㄟ^(guò)減少腦血流或血糖水平來(lái)減少其輸送會(huì)減弱酸中毒的發(fā)展。我們之前已經(jīng)表明,在我們的PA模型中不會(huì)發(fā)生顯著的腦缺血,因?yàn)樵诖蠖鄶?shù)動(dòng)物中,20分鐘PA期間MABP的下降(圖4)未達(dá)到血流自動(dòng)調(diào)節(jié)的下限。誠(chéng)然,我們模型中的PA持續(xù)時(shí)間不足以發(fā)展為嚴(yán)重窒息嬰兒常見的高碳酸血癥和心動(dòng)過(guò)緩,然而,它可以很好地代表心血管適應(yīng)機(jī)制耗盡之前的PA階段,并且可能發(fā)生最顯著的pHbrain改變。總之,我們當(dāng)前的研究提供了新的令人信服的實(shí)驗(yàn)證據(jù),表明不僅是腦缺血,而且結(jié)合臨床相關(guān)水平的低氧、高碳酸血癥和高血糖的真正PA足以引發(fā)足夠嚴(yán)重(pHbrain<6.0)以強(qiáng)烈影響神經(jīng)元存活的腦酸中毒。發(fā)展的pHbrain和pHa之間≥0.8個(gè)pH單位的差異表明跨血腦屏障的H?梯度>6倍,這與之前的發(fā)現(xiàn)一致,即新生豬的血腦屏障是成熟的,并且未因PA而嚴(yán)重受損。
pHbrain的改變不僅在急性PA期間發(fā)揮重要作用,在復(fù)蘇/再氧合后也具有重要病理生理學(xué)意義。先前的研究報(bào)道仔豬在從PA恢復(fù)后pHbrain保持穩(wěn)定,但未對(duì)恢復(fù)4小時(shí)后的情況進(jìn)行隨訪。相反,我們當(dāng)前的研究將窒息后觀察期延長(zhǎng)至24小時(shí)。我們發(fā)現(xiàn)在該仔豬PA/HIE模型中,PA后24小時(shí)期間未出現(xiàn)pHbrain的重大繼發(fā)性改變。
我們目前的發(fā)現(xiàn)與先前在仔豬HIE模型中使用MRS獲得的pHi數(shù)據(jù)一致,該模型使用缺氧缺血應(yīng)激而非PA。在該研究中,pHi在缺血應(yīng)激恢復(fù)后48小時(shí)內(nèi)保持在基線水平,此外,繼發(fā)性能量衰竭的發(fā)展并未反映在該時(shí)間段內(nèi)的pHi改變中。一項(xiàng)人類MRS研究也報(bào)道,在出生后第一天,窒息但血碳酸正常的足月新生兒中pHi正常(7.13±0.05),與我們的研究一致。重要的是,腦堿中毒在隨后幾天內(nèi)發(fā)展,并持續(xù)數(shù)周甚至數(shù)月。
然而,我們需要指出,我們的PA/HIE仔豬模型代表了需要插管和呼吸支持但非自主呼吸的窒息嬰兒亞組。雖然機(jī)械通氣嬰兒保持血碳酸正常,但自主呼吸嬰兒經(jīng)常過(guò)度通氣并可能發(fā)展為低碳酸血癥。這種反應(yīng)可能反映了相對(duì)過(guò)度通氣,繼發(fā)于誘導(dǎo)的低氧性低代謝導(dǎo)致CO?產(chǎn)生減少。由于過(guò)度通氣導(dǎo)致的PaCO?降低傾向于升高pHbrain,這一觀點(diǎn)特別值得關(guān)注,因?yàn)榈吞妓嵫Y已被確定為不良神經(jīng)結(jié)局的獨(dú)立危險(xiǎn)因素。在仔豬中,即使沒有窒息,中度低碳酸血癥也足以引起腦灌注減少,同時(shí)pH和乳酸水平升高。確實(shí),我們的發(fā)現(xiàn)間接表明,維持血碳酸正常/輕度高碳酸血癥可能預(yù)防繼發(fā)性pHbrain改變。最近一項(xiàng)旨在建立大鼠和豚鼠出生窒息轉(zhuǎn)化有效小動(dòng)物模型的工作發(fā)現(xiàn),模擬出生窒息期間較高的PaCO?水平以及之后逐漸恢復(fù)血碳酸正常對(duì)腦代謝性酸中毒、氧氣和乳酸水平產(chǎn)生有益影響。顯然,需要進(jìn)一步的研究在仔豬模型中探索這些效應(yīng)。
我們當(dāng)前的研究存在一些額外的局限性。我們僅使用一種窒息水平從新皮層收集pHbrain數(shù)據(jù),未探索其他腦區(qū)和應(yīng)激水平。
結(jié)論
我們的轉(zhuǎn)化性仔豬PA/HIE模型再現(xiàn)了出生窒息的所有主要特征,并在未采用頸動(dòng)脈閉塞和/或出血性低血壓的情況下引發(fā)了顯著的神經(jīng)元損傷。在該模型中,PA期間pHbrain降至6.0以下,比pHa低≥0.8個(gè)pH單位,確立了嚴(yán)重酸中毒在神經(jīng)元損傷中的致病作用。然而,在恢復(fù)基線水平后,在24小時(shí)亞急性期內(nèi)未觀察到繼發(fā)性pHbrain改變,這可能是由于通過(guò)控制機(jī)械通氣預(yù)防了繼發(fā)性低碳酸血癥。
 相關(guān)新聞
相關(guān)新聞