熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
2.3實驗條件的優化
緩沖液的pH值、沉積電位以及沉積時間會直接影響CH3Hg+在金微電極表面的沉積過程,進而影響CH3Hg+檢測的靈敏度。通過考察以上參數對0.50μg/L CH3Hg+溶出峰電流的影響,最終獲得最佳實驗參數,如表1.
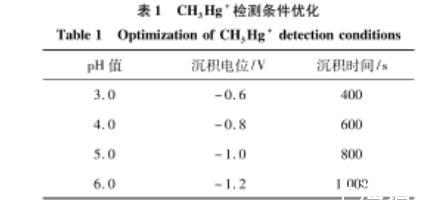
表1 CH3Hg+檢測條件優化
反應條件的優化實驗步驟為:①在沉積電位為——1.0 V、沉積時間為500 s、不同pH值(3.0、4.0、5.0和6.0)條件下,研究金微電極對CH3Hg+的響應情況。實驗得出,在pH=5.0時,所對應的CH3Hg+溶出峰電流最高為0.306 nA,故選用該pH值進行后續實驗。②在緩沖液pH=5.0、沉積時間為500 s條件下,探究在沉積電位為——1.2——0.6 V內金微電極對CH3Hg+的變化。結果發現,當沉積電位為——0.8 V時,CH3Hg+溶出峰電流最高為0.321 nA,因此,將——0.8 V作為最佳沉積電位繼續后續實驗。③在pH=5.0、沉積電位為——0.8 V時,探究沉積時間為400——1200 s(400、600、800、1000和1200 s)內金微電極對CH3Hg+的相應情況。結果發現,適當延長沉積時間有利于CH3Hg+的有效沉積檢測,在沉積時間為800 s時,CH3Hg+溶出峰電流值達到最高值約為0.472 nA.綜上,最終選擇以pH值為5.0、沉積電位為——0.8 V、沉積時間為800 s為最佳實驗條件。
2.4 CH3Hg+在金微電極上的溶出伏安響應
相對其他伏安技術,DPV檢測有較高的靈敏度以及較好的分辨率。在優化后的試驗參數下:pH值為5.0的0.1 mol/L醋酸緩沖液,在——1.0 V沉積電位下富集800 s,不同質量濃度的CH3Hg+在金微電極中的DPV氧化峰電流響應曲線和金微電極對不同質量濃度CH3Hg+的校準曲線,結果如圖3.由圖3(a)不難發現,在金微電極上CH3Hg+于0.56 V處有一個顯著的響應峰,并且隨著CH3Hg+質量濃度的增大而增高。由圖3(b)可見,CH3Hg+的溶出峰電流與其濃度在0.05——0.50μg/L內有很好的線性關系,其線性回歸方程為I=0.354ρ-0.008,通過線性方程斜率計算得出靈敏度為0.354 nA/(μg·L),相關系數為0.998.按照3倍信噪比算法,得出檢測限為0.012μg/L,遠低于世界衛生組織給出的關于飲用水中CH3Hg+質量濃度的指導值(1.0μg/L)。表2為不同電極對CH3Hg+檢測靈敏度的比較,由表2可見,用于檢測CH3Hg+的傳感器相比以往檢測方法更為敏感簡捷,表明金微電極分析檢測具有更廣泛的應用前景。
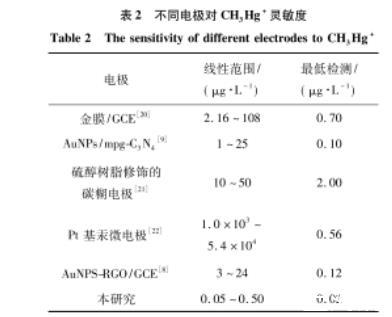
表2不同電極對CH3Hg+靈敏度
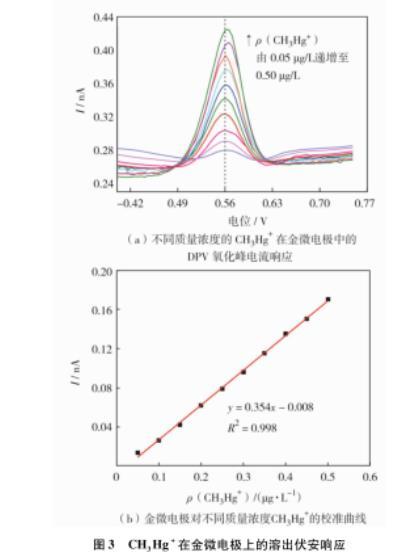
圖3 CH3Hg+在金微電極上的溶出伏安響應
2.5干擾性研究
考慮到實際檢測的水環境要比緩沖溶液成分更復雜,重金屬離子相互干擾現象可能會對檢測結果造成影響。為此,本實驗研究了其他重金屬離子對CH3Hg+檢測的干擾行為,分別加入質量濃度均為40μg/L的兩種重金屬離子(Cu2+和Hg2+),測量CH3Hg+質量濃度為1.0——8.0μg/L時的響應電流變
化。不同質量濃度下CH3Hg+在醋酸緩沖液中的DPV響應如圖4(a)。由圖4(a)可見,CH3Hg+、Cu2+和Hg2+的出峰位置相距較遠,Cu2+和Hg2+的存在并不會對CH3Hg+的檢測產生明顯的影響。CH3Hg+的溶出峰位置在0.60 V左右,隨著CH3Hg+質量濃度的增加,與溶出峰電流呈良好的線性關系,所構建傳感器對CH3Hg+仍保持顯著的電化學信號增量,說明該傳感器選擇性和抗干擾性良好。
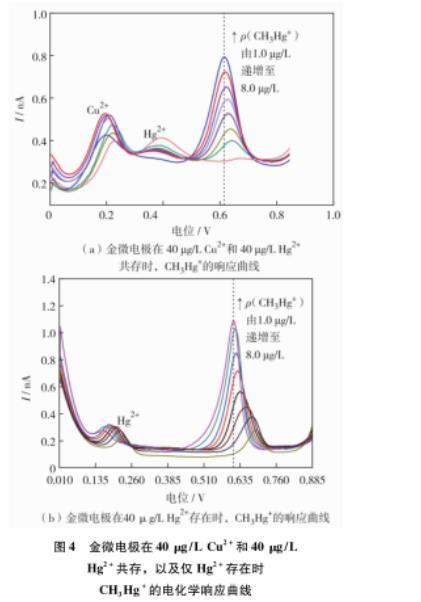
圖4金微電極在40μg/L Cu2+和40μg/L Hg2+共存,以及僅Hg2+存在時CH3Hg+的電化學響應曲線
CH3Hg+檢測的最大干擾離子為無機汞Hg2+,ABOLLINO等采用金納米粒子改性玻碳電極(AuNPS-GCE)研究Hg2+存在的環境下CH3Hg+的伏安行為,實際檢測發現,構筑的電化學傳感器未能實現對CH3Hg+的選擇性分析,二者溶出峰存在重疊現象,添加SnCl2絡合緩沖液中的Hg2+,最終實現了對CH3Hg+的選擇性檢測。KOROLCZUK等開發出一種全氟磺酸——聚四氟乙烯(nafion)修飾金膜電極研究Hg2+存在下CH3Hg+的靈敏分析,通過引入二乙烯三胺五乙酸與汞離子形成絡合物從而減少對CH3Hg+檢測的影響。本研究構筑的金微電極可直接實現對僅Hg2+存在下的CH3Hg+選擇性分析。如圖4(b),隨著CH3Hg+的持續加入(ρ(CH3Hg+)為1.0——8.0μg/L),金微電極上的CH3Hg+沉積量增多,溶出電流逐漸增大,峰值電流高于無Hg2+情況下的電流值,呈現較好的線性關系,而Hg2+的溶出峰幾乎無明顯變化。這是因為金微電極獨特的靈敏性以及金具有的超高導電性,致使其能很敏感地檢測到CH3Hg+與無機汞離子的氧化性差異,在一定的酸性條件下,能將二者很好的區分出來。研究結果進一步說明用金微電極可以實現CH3Hg+在與單一離子Hg2+共存情況下的無干擾檢測。
2.6電極的重現性測試
在電化學分析中,傳感器的循環重復性能在實際檢測分析中至關重要,將金微電極置于室溫下15 d后,對質量濃度為5.0μg/L的CH3Hg+溶液進行5次連續的平行測定,5次監測數據均顯示CH3Hg+溶出峰電流無明顯變化,其檢測結果的相對偏差為4.23%,重現性良好。同時,為測定該傳感器的穩定性,將金微電極保存在0.1 mol/L ABS緩沖液中,并置于4℃下15 d后,然后每隔3 d進行DPV測試,結果表明,該電極仍然保留94.3%的初始響應值。因此,該金微電極傳感器具有良好的穩定性,可長期使用。
2.7實際樣品分析
為評估該CH3Hg+檢測方法的適用性和準確性,對取自合肥工業大學斛兵塘的水樣以及自來水樣進行檢測。樣品經過簡單的過濾處理后,用0.1 mol/L醋酸緩沖液(pH=5.0)以1∶9(體積比)進行稀釋,利用傳統的玻碳電極對水樣進行檢測時,未檢測出CH3Hg+.而用本研究中的金微電極對水樣進行檢測時發現,當CH3Hg+初始質量濃度為0.015μg/L時,峰值電流為0.02 nA;當CH3Hg+添加質量濃度為0.20μg/L時,峰值電流為0.34 nA.向水樣中滴加CH3Hg+并進行回收率實驗,回收率如表3,這表明該方法可以適用于實際水樣品的超痕量檢測。
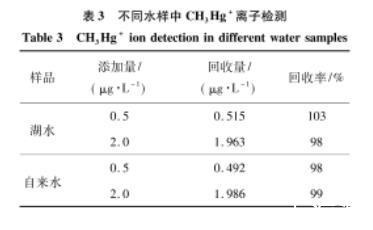
表3不同水樣中CH3Hg+離子檢測
結語
通過對比玻碳電極和金微電極在不加任何修飾劑的情況下對CH3Hg+的伏安響應分析,發現金微電極更為靈敏,最低檢測質量濃度低至0.10μg/L.由于金微電極優異的導電性以及微型傳感器的靈敏性,實現了對目標物CH3Hg+的超痕量檢測,峰值電流與CH3Hg+質量濃度(0.05——0.50μg/L)呈較好的線性關系,檢測限為0.012μg/L.金微電極具有良好的穩定性、重現性和抗干擾性。該檢測機制具有組合方法簡單、響應速度快、檢測限低和取樣少等優點,更加適用于水環境中重金屬離子的痕量檢測。研究數據表明,金微電極聯合微分脈沖伏安技術是檢測水環境中CH3Hg+的有效工具。
 相關新聞
相關新聞