熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
汞廣泛存在于水環(huán)境中,主要形式有元素汞、無機汞和有機汞,是全球性環(huán)境污染物之一。有機汞毒性最強,具有生物累積和放大效應的甲基汞(CH3Hg+)毒性最為致命。日常生活中,人們主要通過食用被污染的海產(chǎn)品接觸CH3Hg+,接觸后CH3Hg+迅速滲透入到皮膚內,直接攻擊人體中樞神經(jīng)系統(tǒng)和腎臟。為避免環(huán)境CH3Hg+對人體的傷害,對CH3Hg+的定量檢測極其重要。
目前,檢測CH3Hg+的方法主要有原子光譜法、電感耦合等離子質譜法、氣相色譜法和電化學傳感器法等。在分析微量目標物方面,光譜法、質譜法和色譜法具有較高的靈敏度,也可對目標物的形態(tài)進行合理分析,但是由于這些非電化學法存在目標物預處理復雜、分析周期長、操作程序復雜、儀器設備昂貴和運行維修成本高等局限,難以滿足對污染物形態(tài)進行現(xiàn)場檢測的迫切需求。電化學檢測法憑借其操作簡單、快速、可靠,以及無需對目標物進行繁瑣預處理操作等優(yōu)勢,有望實現(xiàn)對CH3Hg+形態(tài)的現(xiàn)場快速分析。
與傳統(tǒng)固體電極相比,微電極具有較小電極面積、目標物取樣少、檢測限低、響應速率快、雙層電容以及充電電流小等獨特電化學特性,在痕量分析中受到廣泛關注。DU等合成制備石墨烯微電極用于動物神經(jīng)活動分析研究。GIBBON-WALSH等以金絲微電極對海水以及未污染的地下水中砷的痕量進行檢測,構建的負載錳金絲微電極可有效用于As5+超痕量檢測。RIBEIRO等探究CH3Hg+在碳纖維電極上的電化學行為,運用循環(huán)伏安及快速線性掃描技術探究氯酸環(huán)境下的CH3Hg+,該檢測技術可達到微摩爾級別。
目前,有關電化學檢測CH3Hg+的報道主要采用納米材料改性傳統(tǒng)電極展開,而金微電極直接痕量檢測CH3Hg+的卻鮮有報道。CHEN等合成AuNPs/mpg-C3N4納米復合電化學傳感器用于甲基汞定量分析,獲得較低檢測限0.103μg/L.ABOLLINO等運用高導電性金納米粒子修飾玻碳電極測定甲基汞。
以上檢測CH3Hg+的方法,在實際水樣檢測中要達到相應的檢測效果,主要通過負載(納米)材料改性電極實現(xiàn)。但由于改性材料合成步驟復雜,檢測時穩(wěn)定性不夠,實際檢測中易出現(xiàn)電極表面材料脫落現(xiàn)象,導致檢測限和檢測靈敏度不佳。基于以上問題,本研究提出采用預處理活化后的金微電極直接微分脈沖伏安法測定水環(huán)境中的CH3Hg+,借助金與汞的特殊親和作用,避免了修飾材料的不可控因素,更易實現(xiàn)對CH3Hg+的高穩(wěn)定性、高選擇性、低檢測限的超痕量檢測(檢測濃度≤0.10μg/L)。
1實驗
1.1儀器和試劑
所有伏安檢測均在電化學工作站(購自上海辰華公司,型號為CHI660D)上進行;實驗所需器材:P-2A型金相試樣拋光機、金微電極(直徑25μm,純度99.99%,硬)、玻碳電極(直徑3 mm)、鉑絲對電極、Ag/AgCl參比電極的三電極系統(tǒng)和智能恒溫控制攪拌器。所有測量均在室溫下的10 mL電解質溶液中進行。實驗所需藥品:不同粒徑的氧化鋁粉末、0.5 mol/L H2SO4溶液、0.1 mol/L不同pH值(3.0——6.0)的醋酸緩沖液(由0.1 mol/L CH3COOH以及0.1 mol/L的CH3COONa按體積比例配置),均購自上海化學試劑公司。CH3Hg+標準儲備溶液:由氯化甲基汞(methylmercury chloride,購自中國阿拉丁公司)溶于超純水中制備CH3Hg+原液。實驗所用藥品均為分析純,所制溶液均為超純水配制。
1.2電極預處理
分別采用粒徑為1.00、0.30和0.05μm氧化鋁粉末依次將工作電極拋光至鏡面,使電極表面平滑,再浸入乙醇水溶液(體積分數(shù)為50%)和去離子水中超聲數(shù)分鐘,去除電極表面附著的雜質。隨后置于室溫下風干備用。玻碳電極和金微電極測定CH3Hg+之前均需活化處理,即將工作電極置于酸性溶液中,用循環(huán)伏安法掃描直至獲得穩(wěn)定的伏安曲線,以增加電極表面活點密度以及促進電子轉移速率,從而增強電催化性能。具體操作如下:將三電極系統(tǒng)置于0.5 mol/L的H2SO4溶液中,——0.2——1.6 V循環(huán)掃描15圈,掃描速度設定為100 mV/s,直到獲得穩(wěn)定的循環(huán)伏安曲線。隨后將金微電極、玻碳電極用超純水沖洗干凈,在氮氣氛下烘干備用。
1.3電化學實驗
采用微分脈沖伏安技術(differential pulse voltammetry,DPV)對CH3Hg+進行電化學分析。將標準三電極系統(tǒng)浸入含有CH3Hg+的電解質溶液中,以預處理活化的兩根電極為工作電極。脈沖伏安法檢測依據(jù)重金屬陽離子的氧化還原反應,主要分為目標離子沉積、電化學檢測和解吸3個階段。具體操作為:①給工作電極施加一個負電位,促使分散在電解液中的CH3Hg+通過還原反應沉積在工作電極表面,為保證沉積的有效性,沉積階段電解液一直處于攪拌狀態(tài),轉速為500 r/min,沉積一段時間后,攪拌終止;②靜息平衡15 s后記錄下伏安圖;③施加一個解吸電位使得第1階段沉積的物質再次得到電子,氧化成最初的陽離子,即由氧化還原反應引起的電子定向移動,電化學工作站記錄下峰值電流。最終得出響應曲線。
為便于分析金微電極對CH3Hg+的電分析性能,采用DPV研究不同電極在質量傳輸以及電子轉移方面的差異,以及在相同濃度下,金微電極和玻碳電極對CH3Hg+的溶出伏安響應情況,優(yōu)化實驗條件后,選用金微電極作為DPV檢測CH3Hg+的工作電極,并得出最佳檢測靈敏度以及最低檢測限。
2結果與討論
2.1預處理金微電極的電化學行為
圖1分別是預處理金微電極和玻碳電極在0.5 mol/L H2SO4溶液中的循環(huán)伏安曲線(初始電位為——0.20 V)。由圖1(a)可知,金微電極于0.90 V產(chǎn)生較大的特征還原峰,于1.20 V產(chǎn)生氧化峰。響應峰分別對應于金微電極表面金屬氧化物的還原以及金屬氧化物的形成。由圖1(b)可知,玻碳電極的CV曲線是一對可逆的氧化還原反應,但峰形效果不好,相同條件下金微電極的CV曲線更為尖銳。氧化還原曲線具有更高的峰值電流,這主要是因為金微電極具有優(yōu)異的導電能力。
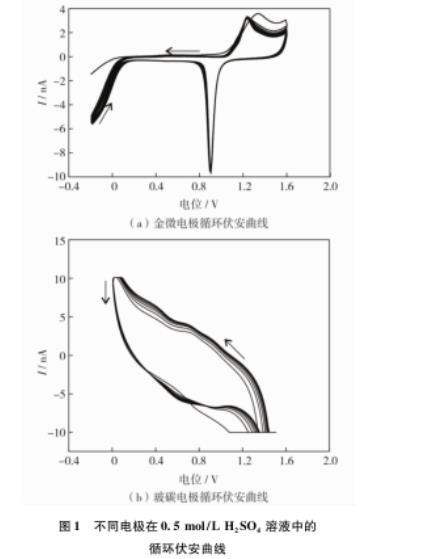
圖1不同電極在0.5 mol/L H2SO4溶液中的循環(huán)伏安曲線
2.2玻碳電極、金微電極對CH3Hg+的伏安分析
CH3Hg+的伏安測定通常是基于CH3Hg+自由基發(fā)生的可逆波,而可逆波的大小和形狀及重現(xiàn)性會受到工作電極表面修飾的顯著影響。在預沉積階段,CH3Hg+在工作電極表面富集,短時間靜息平衡后,再清洗電極除去工作電極表面的沉積物。CH3Hg+在工作電極表面的反應原理為
 (1)
(1)
相同實驗條件下,玻碳電極和金微電極對CH3Hg+的靈敏性檢測如圖2.由圖2(a)可見,金微電極對不同質量濃度(0.1,0.2,0.3,0.4,0.5,0.6,0.7,0.8μg/L)CH3Hg+的DPV響應,并在每個濃度下均出現(xiàn)明確的響應峰。CH3Hg+在金微電極上于0.68 V位置處出現(xiàn)響應峰,并且隨著CH3Hg+質量濃度的增大而增高,溶出峰電流逐漸正移,與CH3Hg+質量濃度呈較好的線性關系。其線性回歸方程為I=0.283ρ-0.023,在CH3Hg+質量濃度僅為0.1μg/L的水環(huán)境下能出現(xiàn)響應峰。由此可知,金微電極可以于實現(xiàn)CH3Hg+的超痕量檢測。
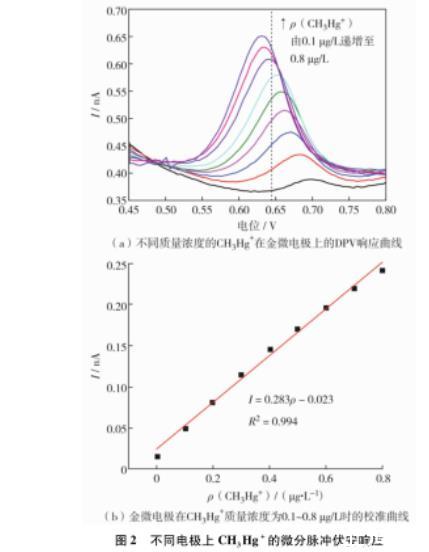
圖2不同電極上CH3Hg+的微分脈沖伏安響應
 相關新聞
相關新聞