熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
研究簡介:在完整的腦中,存在一個復雜的系統來協調能量底物的輸送,并根據神經元的能量代謝需求調整能量底物池的組成。然而,在體外的腦切片實驗中,這種復雜的系統并不存在,神經元的能量供應完全依賴于實驗條件。因此,確保實驗條件盡可能接近體內情況是體外研究的首要要求,其中氧氣供應是關鍵因素之一。標準人工腦脊液(ACSF)中僅含有葡萄糖作為能量底物,但體內腦組織中的能量底物池可能更為復雜,包括乳酸等其他底物。本論文主要研究了腦切片中能量代謝的臨界狀態,重點探討了氧氣輸送和能量底物在塑造神經元活動中的關鍵作用。研究人員使用了P19至P44的瑞士小鼠海馬腦切片。通過施加不同頻率的刺激,記錄局部場電位(LFPs)和NAD(P)H熒光變化,同時測量切片組織中的氧分壓(pO2)。實驗中,通過改變灌流速率(4ml/min和15ml/min)來研究氧氣供應對神經元活動的影響,并比較了在標準ACSF和富含能量底物的ACSF(eACSF,包含葡萄糖、丙酮酸、β-羥基丁酸等)中的神經元活動和能量代謝。本研究表明,腦切片中的神經元活動和能量代謝對氧氣供應極為敏感,且在高氧氣供應下,其他能量底物可以增強神經元的氧化代謝和功能。然而,在氧氣供應不足時,這些底物的效果大打折扣。因此,在體外腦切片實驗中,確保充足的氧氣供應和合理選擇能量底物對于模擬體內神經元活動至關重要。
Unisense微電極系統的應用
Unisense微電極被用于測量腦切片組織中的氧分壓(pO2)。具體使用的是Clark式氧氣微電極,其尖端直徑為10微米。該微電極連接到PA2000主機上,用于精確測量切片組織中的氧氣濃度。使用了兩點校準法,將電極插入33°C的生理鹽水溶液中,分別在95%氧氣或環境空氣中平衡,以校準電極。氧氣微電極被放置在與場電位記錄電極相近的位置,用于測量局部組織氧分壓的變化。通過Unisense微電極,研究人員能夠實時、高精度地測量切片組織中的氧分壓,采集到的數據用于分析氧氣供應對神經元活動的影響,特別是在不同灌流速率下氧氣分布的變化。
實驗結論
研究結果證實,在急性腦組織切片中,決定神經元興奮性的基本神經元參數與氧化能代謝密切相關。我們還表明,能量代謝狀態對切片組織中氧氣的可用性高度敏感。這個ATP合成途徑在腦組織切片中顯然受到了損害,因此神經元活動對氧濃度的依賴性明顯轉向了更高的氧分壓值。此外,在神經元活動期間,葡萄糖可能無法完全滿足神經元的能量需求,因此還需要其他與葡萄糖互補的能源物質來為氧化代謝提供充分的支持。鑒于在眾多電生理學研究中,切片中的氧分壓以及腦灌注液中的能量物質組成均未得到控制。
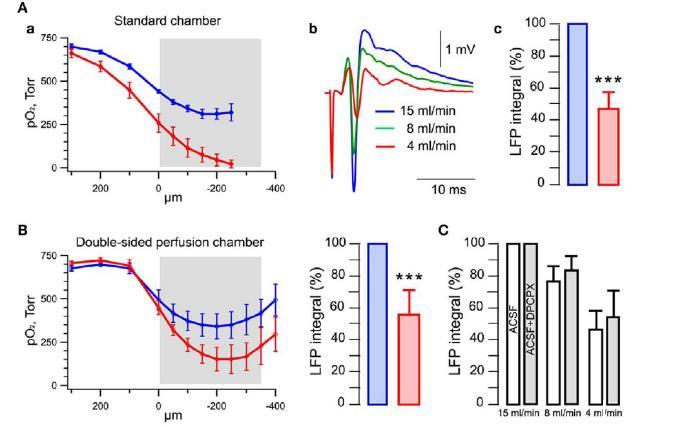
圖1、灌流速率對切片氧分壓和LFP幅度的影響。A)氧分壓深度分布,(a):展示了在15ml/min和4ml/min灌流速率下,腦切片中的氧分壓深度分布。圖中灰色條表示切片的位置。在15ml/min時,切片核心的氧分壓約為300Torr,而4ml/min時,切片核心的氧分壓急劇下降。(b)在CA1區記錄的LFPs,由單次刺激Schaffer collateral(SC)引起。LFPs的幅度在15ml/min時顯著高于4ml/min。(c)統計總結了不同灌流速率下LFP積分值的變化。15ml/min時的LFP積分值顯著高于4ml/min。B)雙層灌流室中的氧分壓。C)阿登苷酸受體拮抗劑DPCPX對LFP的影響。
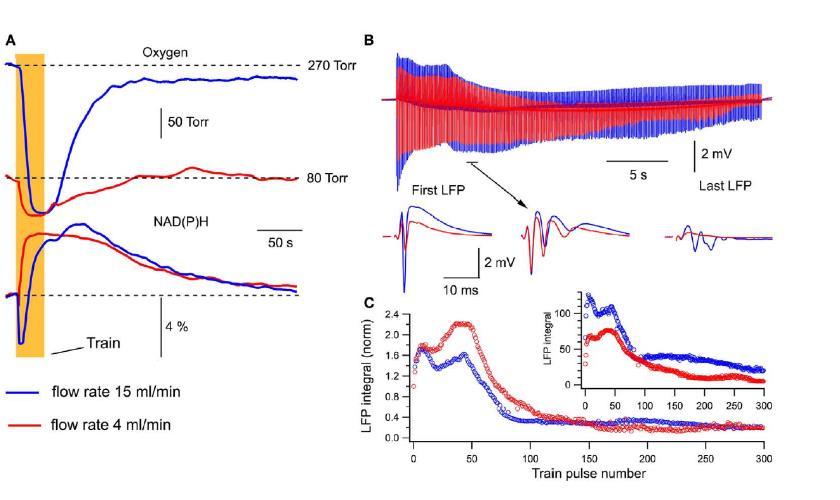
圖2、刺激協議中的局部場電位和氧分壓動態。A.氧分壓和LFPs的同步記錄。展示了在15ml/min灌流速率下,通過一系列單次SC刺激(1/7s)激活神經元后,30秒10Hz刺激引起的氧分壓和LFPs的動態變化。B.氧分壓和LFPs的時間過程。展示了氧分壓和LFPs隨時間的變化過程,進一步說明了兩者之間的相關性。
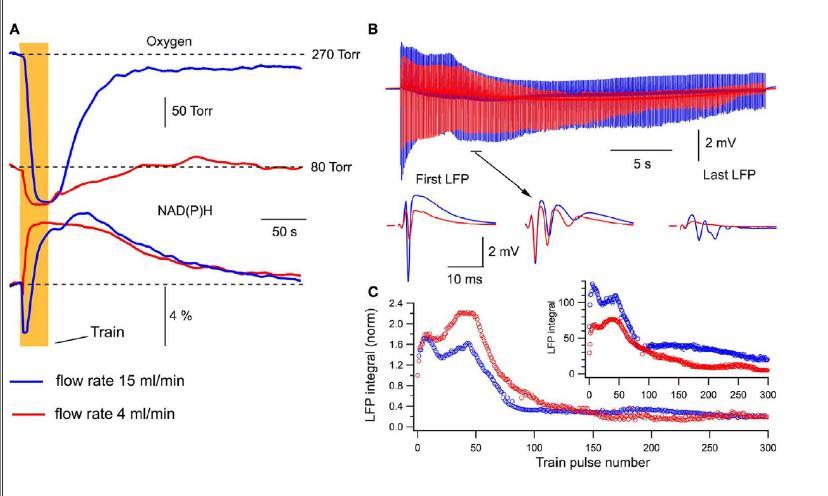
圖3、不同灌流速率下的氧分壓、NAD(P)H信號和LFPs。A)氧分壓和NAD(P)H自熒光。展示了在15ml/min和4ml/min灌流速率下,氧分壓和NAD(P)H自熒光的變化。B)LFPs在刺激訓練中的變化。展示了在不同灌流速率下,LFPs在30秒10Hz刺激訓練中的變化。C)LFPs積分值的比較。展示了不同灌流速率下,LFPs積分值的變化。在4ml/min時,LFPs積分值顯著下降。
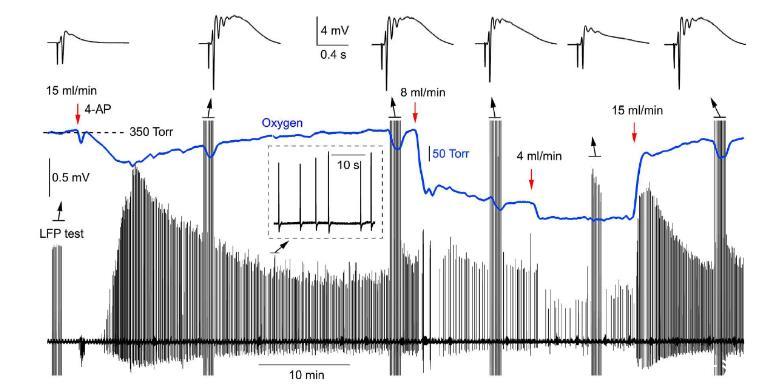
圖4、4-AP誘導的同步網絡活動對灌流速率的依賴性。展示了在不同灌流速率下,4-AP誘導的同步網絡活動的LFPs和氧分壓的變化。
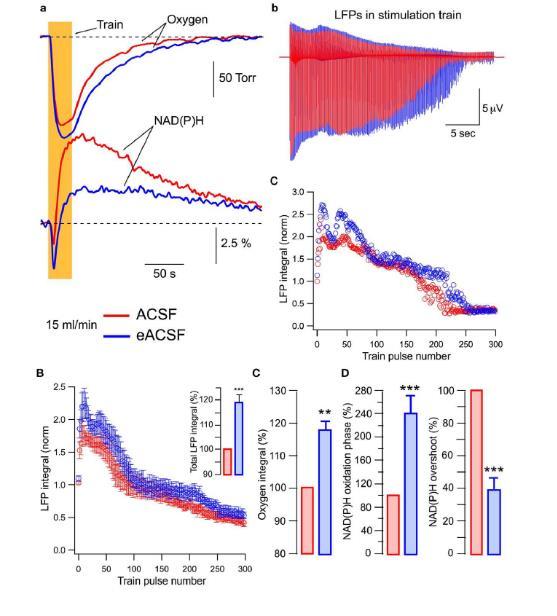
圖5、在充足氧氣供應下,富含能量底物的ACSF增強氧化代謝和突觸功能。A)氧分壓和NAD(P)H瞬態以及LFPs,展示了在富含能量底物的ACSF(eACSF)中,30秒10Hz刺激引起的氧分壓和NAD(P)H自熒光的變化,以及LFPs的動態變化。B)LFPs積分值,展示了在eACSF中,LFPs積分值的變化。在eACSF中,LFPs的幅度顯著增加。C)氧分壓和NAD(P)H信號參數。展示了在eACSF中,氧分壓和NAD(P)H信號參數的變化。
結論與展望
大腦中的血管-神經-神經膠質相互作用系統能夠控制大腦的能量供應,而在培養皿中這一系統是不存在的,因為能量供應是由實驗條件決定的。盡管神經元活動極其耗能,但關于浸沒腦切片中的能量代謝狀態卻鮮有報道。由于缺乏這些信息,隨意選擇的氧合和代謝條件使得在切片中的有效氧化代謝變得不可靠。研究表明,在小鼠海馬切片(出生后第19-44天)中,誘發的神經元放電、自發的網絡活動(由4-氨基吡啶引發)以及突觸刺激誘導的NAD(P)H胞質熒光強烈依賴于氧氣供應情況。只有當灌注速率高達約15毫升/分鐘(95%氧氣)時,才能為切片提供適當的氧氣供應。較低的氧合會導致局部場電位和自發網絡活動的減少,以及短期突觸可塑性的顯著調節。氧氣供應的減少顯著抑制了NAD(P)H信號的氧化階段,表明神經元活動的變化與有氧能量代謝的減少是平行的。與體內條件相比,神經元活動對氧張力的依賴性在切片中明顯向更高的氧濃度方向轉移。高灌注率提供的充足的氧氣量、將腦灌注液中的葡萄糖部分替換為β-羥基丁酸、丙酮酸或乳酸,都能增強氧化代謝和突觸功能。這表明大腦中高氧含量是維持氧化代謝的必要條件,而僅靠葡萄糖無法滿足神經活動期間的能量需求。研究結果表明,能量代謝決定了神經網絡的功能狀態,這突顯了在體外實驗中必須確保提供充足的代謝支持。
 相關新聞
相關新聞