熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
研究簡介:傳統的藥物治療癌癥不可避免地會帶來毒副作用,并且藥物療效受限于藥物劑量。盡管納米載體的發展在一定程度上改善了這些問題,但仍然存在藥物載荷能力有限的挑戰。因此,研究者們提出了“無藥物治療”的概念,即不使用傳統藥物,而是利用納米催化劑在治療過程中不斷生成治療性物質,從而實現可持續的治療效果。研究者開發了一種Z型結構的SnS1.68-WO2.41納米催化劑。這種催化劑能夠在近紅外光(NIR)照射下生成氧化空穴和氫分子,用于聯合空穴/氫治療。SnS1.68具有窄帶隙(1.49 eV),能夠吸收NIR光并產生氫氣;而WO2.41納米點具有高氧化能力,能夠氧化腫瘤內的過量谷胱甘肽(GSH),從而破壞腫瘤微環境。在NIR光照射下,WO2.41納米點產生的熱電子通過Z型結構注入到SnS1.68納米片中,從而實現高效的光催化氫氣生成和GSH氧化。這種聯合治療策略通過消耗GSH和生成氫氣,抑制癌細胞的能量代謝,破壞細胞的抗氧化防御系統,從而誘導腫瘤細胞凋亡。
通過細胞實驗驗證了SnS1.68-WO2.41納米催化劑在NIR光照射下的細胞攝取、細胞毒性、對線粒體和DNA的損傷作用,以及對細胞內ATP和ROS水平的影響。本研究提出了一種基于光催化的無藥物治療癌癥的新策略,通過聯合空穴和氫治療,實現了高效、低毒的腫瘤治療效果。這種方法不僅避免了傳統藥物治療的毒副作用,還利用了腫瘤內源性物質(如GSH)作為治療靶點,具有廣闊的應用前景。
Unisense氫氣微電極的應用
丹麥Unisense微電極被用于檢測氫氣的生成。將反應溶液(包含納米催化劑和10μM的GSH)與檢測溶液通過分子量為3000 Dalton的濾膜隔開,以避免納米顆粒對電極表面光電效應的干擾。通過Unisense氫氣微電極實時監測氫氣的生成情況。Unisense微電極測量的氫氣生成數據直接證明了SnS1.68–WO2.41納米催化劑在NIR光照射下能夠高效地產生氫氣,且生成速率與激光功率密度呈正相關。這一結果驗證了納米催化劑的光催化性能,表明其在光催化氫氣生成方面具有高效性和可控性。通過實時監測氫氣的生成,證明在無藥物輔助的情況下,納米催化劑能夠通過光催化反應產生具有治療效果的氫氣。這為無藥物治療癌癥的策略提供了有力的實驗支持,展示了該策略在實際應用中的可行性和潛力。氫氣的生成與GSH的消耗相結合,為本論文的研究者提供了關于納米催化劑如何通過聯合空穴/氫治療機制破壞腫瘤細胞能量代謝和抗氧化防御系統的直接證據。
實驗結論
提出了一種基于光催化的無藥物治療癌癥的新概念,即利用納米催化劑在近紅外光(NIR)照射下生成氧化空穴和氫分子,實現聯合空穴/氫治療。這種策略不依賴傳統藥物,避免了藥物治療帶來的毒副作用,同時利用腫瘤內源性物質(如谷胱甘肽,GSH)作為治療靶點,具有可持續性和高效性。開發了一種Z型結構的SnS1.68-WO2.41納米催化劑,該催化劑在NIR光照射下能夠高效地生成氫氣和氧化GSH。SnS1.68具有窄帶隙(1.49 eV),能夠吸收NIR光并產生氫氣;而WO2.41納米點具有高氧化能力,能夠氧化GSH,破壞腫瘤微環境。
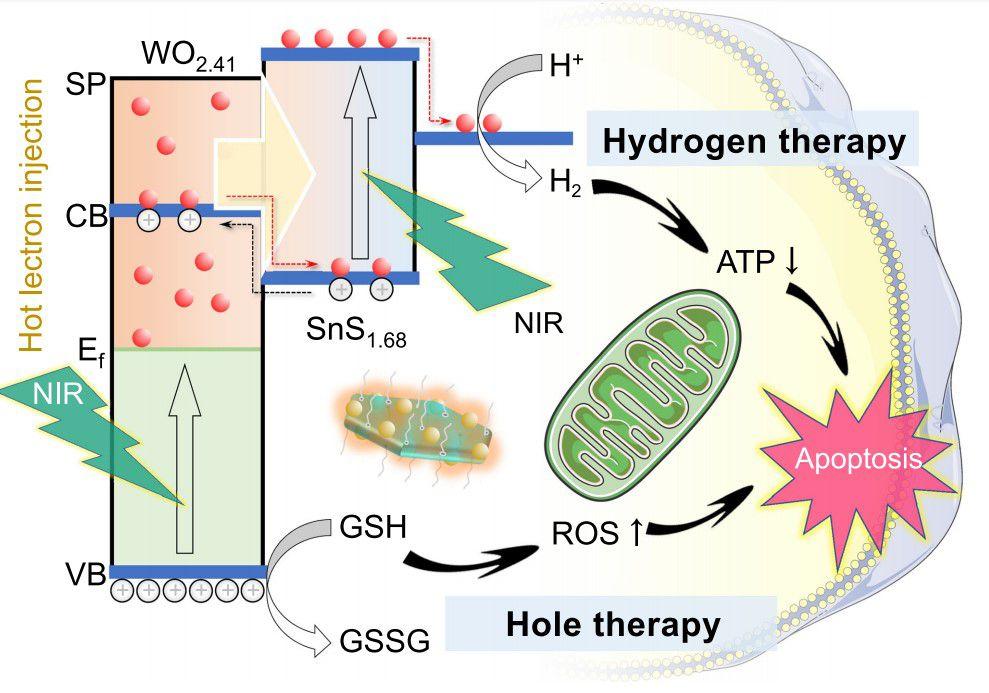
圖1、NIR激活的Z型SnS1.68–WO2.41納米催化劑的空穴/氫氣聯合治療策略和機制的示意圖。
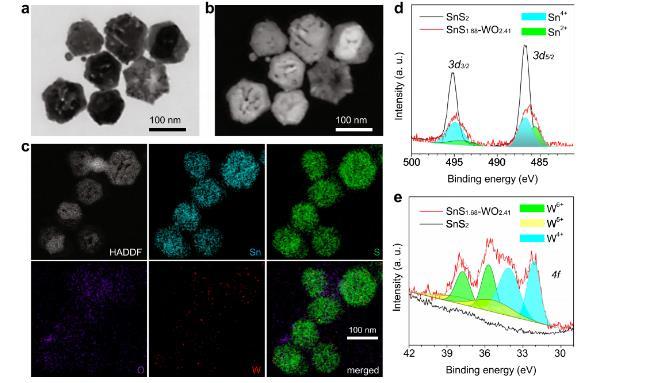
圖2、SnS1.68–WO2.41納米催化劑的形貌、組成和尺寸表征。(a)SEM圖像;(b)對應的STEM圖像;(c)HADDF圖像及元素分布圖;(d,e)SnS?.??–WO?.??納米催化劑的XPS圖譜。這些實驗均獨立重復三次,結果相似。
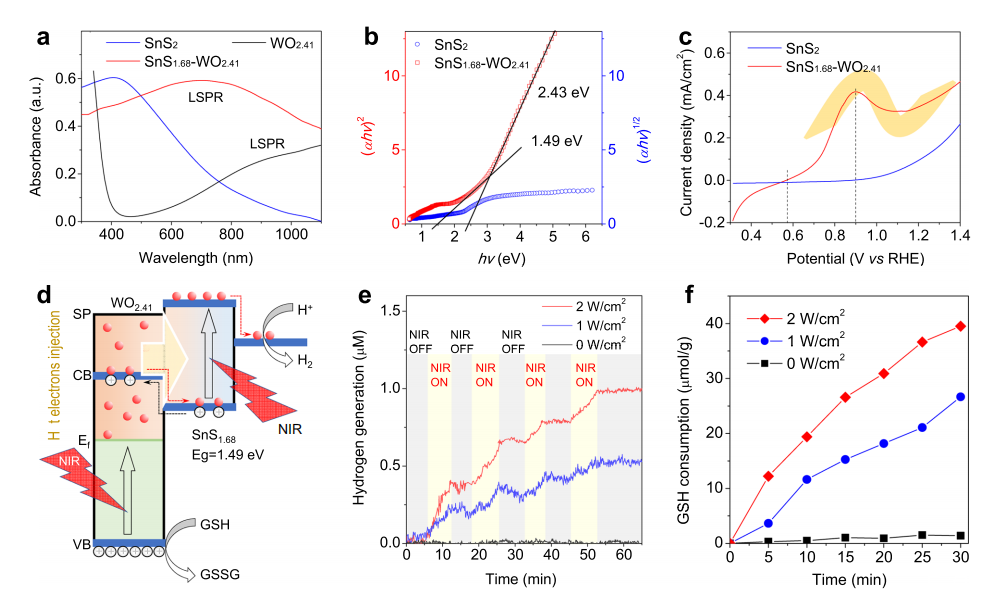
圖3、SnS?.??–WO?.??納米催化劑的光電特性及NIR光催化氫氣生成和GSH消耗性能。(a)UV–VIS–NIR吸收光譜;(b)SnS?和SnS?.??–WO?.??的(αhν)1/2和(αhν)2隨能量(hv)變化的帶隙曲線;(c)SnS?和SnS?.??–WO?.??在808 nm激光照射下的光電流密度–電壓(vs.RHE)曲線;(d)NIR光催化氫氣生成和GSH消耗的機制示意圖;(e)SnS?.??–WO?.??納米催化劑在GSH(10μM)水溶液中808 nm激光照射下,不同功率密度條件下的NIR光催化氫氣生成行為;(f)808 nm激光照射下,不同功率密度條件下的SnS?.??–WO?.??納米催化劑的NIR光催化GSH消耗行為。(a,e,f)圖中的實驗均獨立重復三次,結果相似。
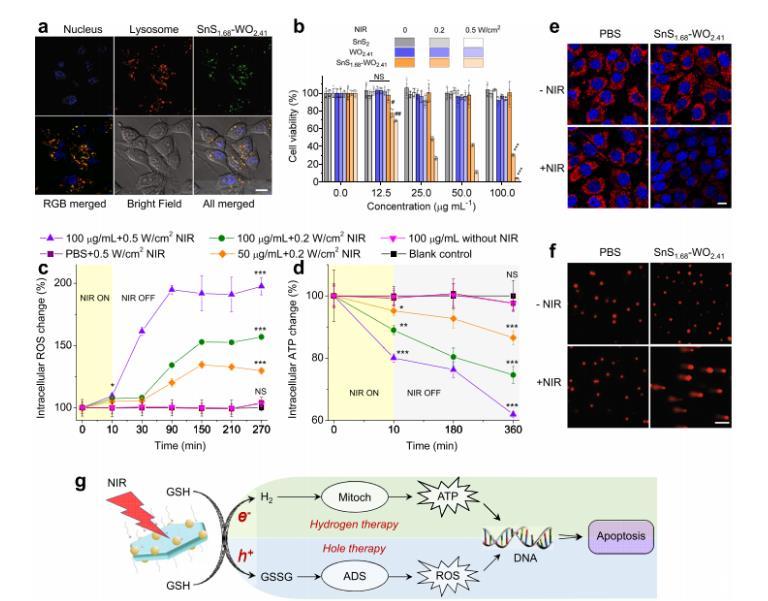
圖4、SnS1.68–WO2.41納米催化劑的空穴/氫氣聯合治療表現與機制。(a)SnS?.??–WO?.??納米催化劑在細胞內培養4小時后的攝取行為;(b)在有/無NIR照射(808 nm,0.2或0.5 W/cm2,10分鐘)的條件下,SnS?.??–WO?.??納米催化劑對4T1細胞的細胞毒性(n=5個生物學獨立樣本);(c)在有/無NIR照射條件下,SnS?.??–WO?.??處理的4T1細胞內ATP水平的監測(n=6個生物學獨立樣本);(d)ROS水平的監測(n=6個生物學獨立樣本);(e)SnS?.??–WO?.??+NIR處理對線粒體的影響(實驗獨立重復三次,結果相似);(f)SnS?.??–WO?.??+NIR處理對4T1細胞DNA的影響;(g)基于SnS?.??–WO?.??納米催化劑的空穴/氫氣聯合治療的機制示意圖。
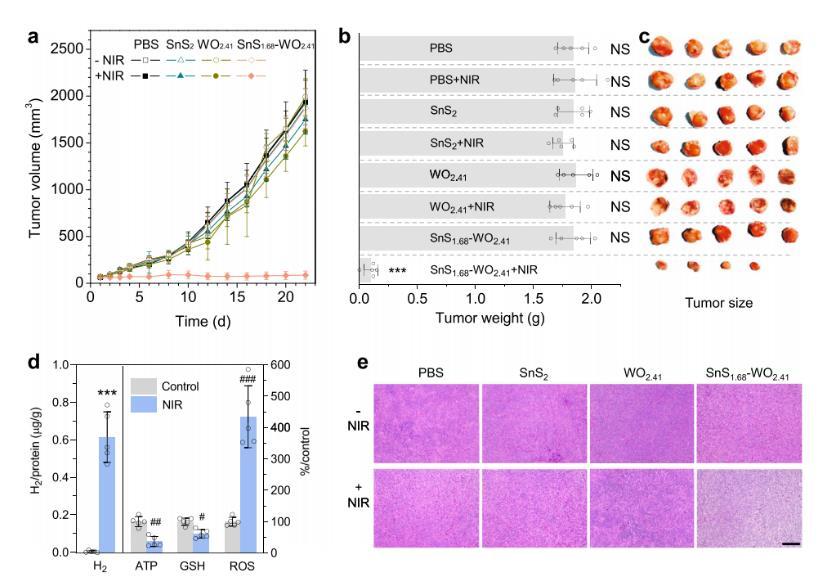
圖5、SnS1.68–WO2.41納米催化劑的體內空穴/氫氣聯合治療表現。(a)4T1腫瘤體積的監測;(b)經22天治療后提取的4T1腫瘤的重量;(c)4T1腫瘤的大小(n=5個生物學獨立樣本);(d)對納米催化劑處理的小鼠,在NIR照射(20分鐘,0.5 W/cm2)前后的腫瘤內H?、ATP、GSH和ROS水平(n=5個生物學獨立樣本);(e)HE染色的腫瘤組織切片。
結論與展望
許多納米載體被開發出來,在一定程度上改善了藥物的副作用和藥效限制,但藥物治療仍不可避免地帶來毒副作用和藥效有限的問題。在這項工作中,研究人員提出了一種無藥物治療的概念,并將其定義為一種治療方法,在治療過程中不使用傳統的有毒藥物,也不消耗治療劑,但具有源源不斷的治療能力,最大化治療效果。通過一鍋法開發了Z型結構SnS1.68–WO2.41納米催化劑,實現了NIR光催化生成孔和氫分子的聯合孔/氫治療。WO2.41納米點通過Z型路徑輕松產生大量熱電子,并將其注入對NIR敏感的SnS1.68納米片,從而實現高效的NIR光催化。SnS1.68–WO2.41納米催化劑在體內外均表現出可控的NIR光催化氫氣生成和GSH氧化,并通過抑制癌細胞能量代謝、提高腫瘤內ROS水平和誘導DNA損傷有效殺死癌細胞和抑制腫瘤生長。Unisense微電極測量的氫氣生成數據直接證明了SnS1.68–WO2.41納米催化劑在NIR光照射下能夠高效地產生氫氣,且生成速率與激光功率密度呈正相關。實時監測氫氣的生成,能夠證明在無藥物輔助的情況下,納米催化劑能夠通過光催化反應產生具有治療效果的氫氣。通過無藥物治療策略,納米催化劑在癌癥治療的療效和生物安全性方面獲得了顯著好處。總的來說,基于催化劑的無藥物聯合治療策略是一種有前景的臨床癌癥治療方法。提出的基于催化的無藥物治療策略為實現癌癥治療的高效性和低毒性開辟了一條新途徑。