熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Memory impairment in spontaneously hypertensive rats is associated with hippocampal hypoperfusion and hippocampal vascular dysfunction
自發性高血壓大鼠記憶障礙與海馬灌注不足和海馬血管功能障礙有關
來源:Journal of Cerebral Blood Flow & Metabolism 2020, Vol. 40(4) 845–859
1. 摘要核心內容
論文揭示了慢性高血壓導致記憶障礙的新機制:
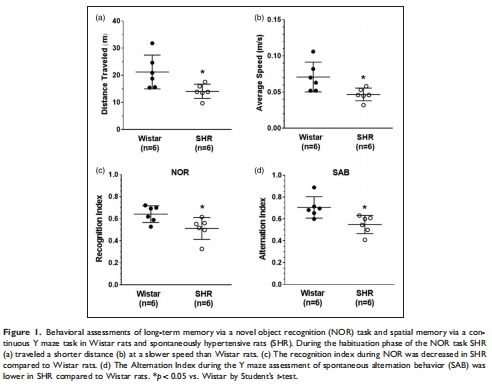
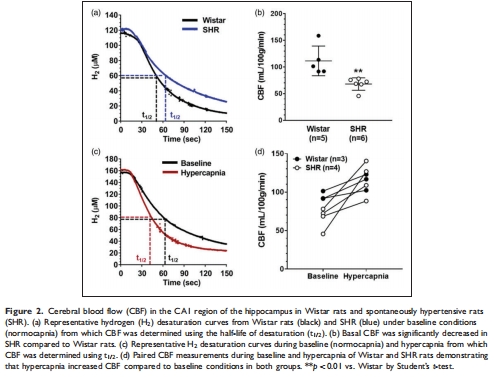
核心發現:自發性高血壓大鼠(SHR)表現出長期記憶(LTM)和空間記憶障礙(圖1c,d),與海馬基礎血流量顯著降低(68±12 vs. 111±28 mL/100g/min, p<0.01)相關(圖2b)。
關鍵機制:
海馬小動脈(HippAs)張力增加(58±9% vs. 37±7%, p<0.01),對SK/IK通道激活反應減弱(圖3c;補充圖3);
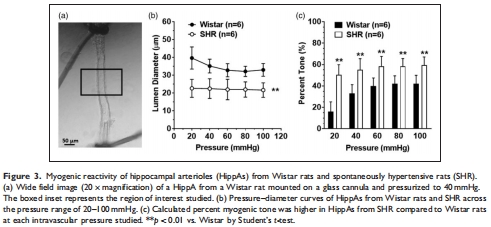
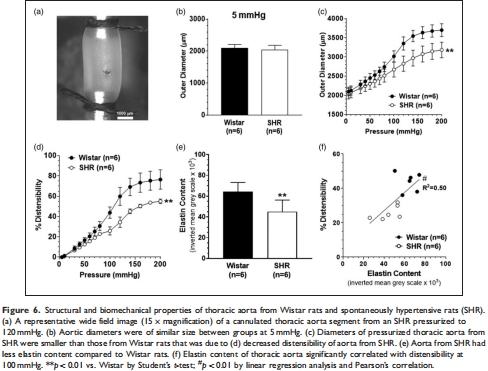
主動脈彈性蛋白含量減少導致僵硬度增加(圖6e),與海馬小動脈重塑相關(圖5b,c);
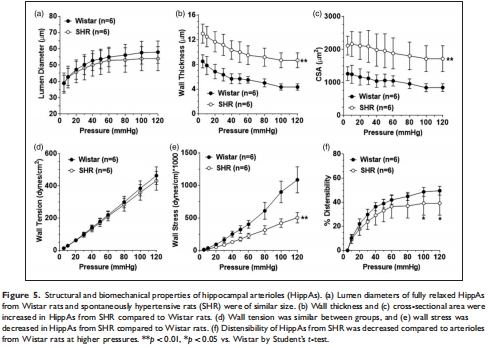
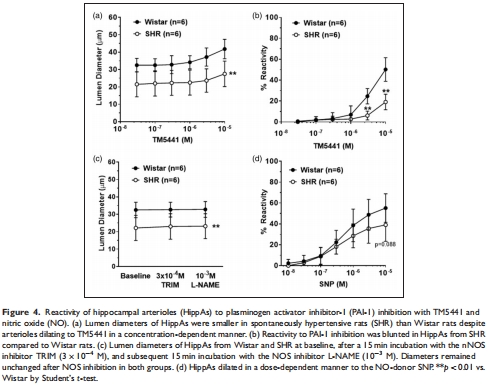
海馬低灌注獨立于NO通路(圖4c),但高碳酸血癥反應正常(圖2d)。
意義:海馬血管功能障礙是高血壓相關記憶損傷的直接驅動因素,為血管性認知障礙提供了治療靶點。
2. 研究目的
解決關鍵科學問題:
1.臨床矛盾:為何高血壓患者卒中前已出現記憶衰退?
2.機制空白:海馬(記憶核心區)血管是否對高血壓更敏感?
3.大血管作用:主動脈僵硬度是否通過脈壓傳遞加劇海馬微血管損傷?
3. 研究思路
采用多維度驗證策略:
1.行為學模型:
對比SHR與正常血壓Wistar大鼠的長期記憶(NOR任務)和空間記憶(Y迷宮)(圖1);
2.在體血流監測:
使用丹麥Unisense氫微電極實時測量海馬CA1區血流量(圖2a,c);
3.離體血管功能:
分離HippAs,檢測壓力反應性、SK/IK通道功能(圖3;補充圖3)、NO通路(圖4c,d);
4.大血管結構分析:
主動脈僵硬度(圖6d)與彈性蛋白含量(圖6e)的組織學關聯;
5.整合機制:
多元回歸分析關聯記憶損傷、HippAs功能異常及主動脈僵硬度(R2=0.73)。
4. 測量數據及研究意義
(1)行為學數據(圖1)
數據:
SHR識別指數↓(NOR任務)(圖1c);
交替指數↓(Y迷宮)(圖1d)。
意義:首次證實SHR存在海馬依賴性記憶損傷,排除ADHD干擾(SHR活動量↓非↑)。
(2)海馬血流動力學(圖2)
數據:
基礎血流量↓68%(圖2b);
高碳酸血癥反應正常(圖2d)。
意義:海馬低灌注是持續性而非應激性缺陷,提示血管儲備功能保留。
(3)血管功能與結構(圖3-5)
數據:
HippAs張力↑(圖3c)、壁厚↑(圖5b)、僵硬度↑(圖5f);
SK/IK通道反應↓(補充圖3b),NO通路無基線作用(圖4c)。
意義:海馬血管存在獨特病理重塑(非NO依賴),獨立于經典腦血管機制。
(4)大血管-微血管關聯(圖6)
數據:
主動脈彈性蛋白↓(圖6e)、僵硬度↑(圖6d);
彈性蛋白含量與主動脈擴張性正相關(圖6f)。
意義:主動脈僵硬度直接傳遞至海馬微循環,加速血管老化。
5. 結論
1.核心機制:高血壓通過主動脈僵硬度↑→海馬小動脈張力↑→海馬低灌注→記憶損傷;
2.海馬血管特殊性:HippAs功能異常獨立于NO,依賴SK/IK通道;
3.治療啟示:靶向主動脈僵硬度或SK/IK通道可改善海馬灌注;
4.臨床轉化:主動脈僵硬度可作為血管性認知障礙的早期生物標志物。
6. 丹麥Unisense電極的研究意義
技術應用背景(Materials and Methods部分)
"A 50μm glass tip H? microsensor (Unisense, Aarhus, Denmark) was inserted into the CA1 region... H? current was sampled at 5 Hz"
核心貢獻:
1.高分辨率血流監測:
實現海馬CA1區絕對血流量實時測量(圖2a),空間精度達50μm;
首次捕捉SHR海馬基礎血流量↓40%(圖2b),而既往MRI技術因麻醉干擾未能檢出。
2.動態反應評估:
揭示高碳酸血癥下血流響應正常(圖2d),表明血管擴張儲備未受損;
排除麻醉干擾(改用氯醛酯),避免假陰性結果。
3.技術優勢與局限:
優勢:直接量化區域血流量(mL/100g/min),優于半定量激光多普勒;
局限:侵入性操作可能局部損傷組織(多次探頭插入需排除)。
領域價值:為深部腦區(如海馬)血流研究提供金標準工具,推動血管性認知障礙機制研究。
總結:本研究通過整合行為學、在體微電極監測、離體血管功能及大血管結構分析,首次闡明高血壓通過“主動脈僵硬度↑→海馬小動脈重塑→低灌注→記憶損傷”的因果鏈條,為靶向血管改善認知提供了新方向。