熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Hydrogen inhibits endometrial cancer growth via a ROS/NLRP3/caspase-1/GSDMD-mediated pyroptotic pathway
氫通過 ROS NLRP3 caspase-1 GSDMD 介導(dǎo)的焦亡途徑抑制子宮內(nèi)膜癌生長
來源:Yang et al. BMC Cancer (2020) 20:28
1. 論文摘要核心內(nèi)容
本研究首次證實 氫氣(H?)通過激活ROS/NLRP3/caspase-1/GSDMD通路誘導(dǎo)子宮內(nèi)膜癌細(xì)胞焦亡(pyroptosis),從而抑制腫瘤生長:
分子機制:氫氣顯著上調(diào)細(xì)胞內(nèi)活性氧(ROS)水平,激活NLRP3炎癥小體,促進caspase-1切割GSDMD蛋白,形成細(xì)胞膜孔洞,導(dǎo)致細(xì)胞焦亡(圖3-6)。
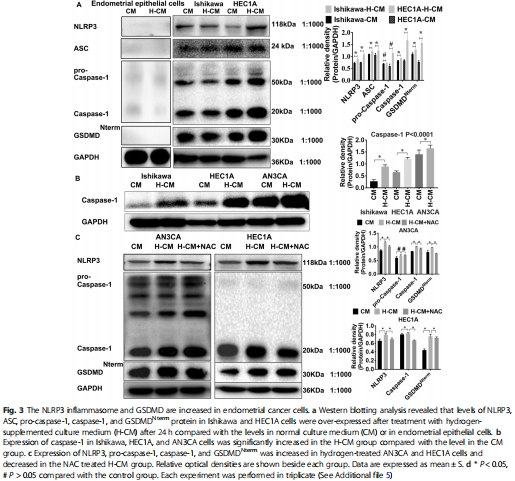
體外驗證:氫氣處理增加PI/TUNEL陽性細(xì)胞(圖5)、LDH釋放(圖6d-f)及IL-1β分泌(圖6g-i),而敲低GSDMD后焦亡被抑制(圖6)。
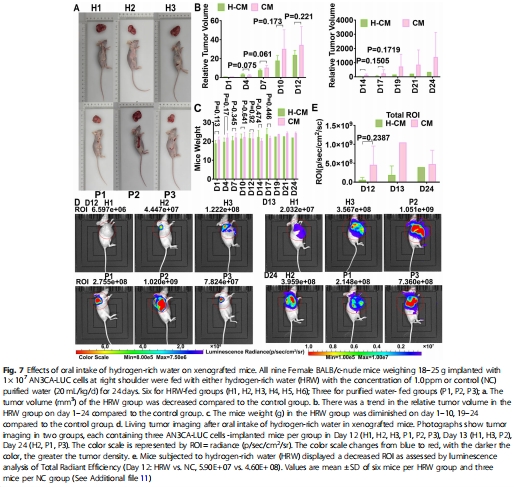
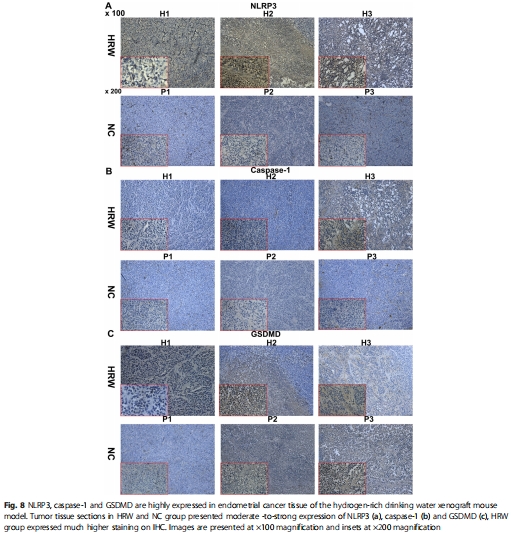
體內(nèi)效果:飲用富氫水(HRW)的小鼠腫瘤體積和重量顯著減小(圖7a-c),腫瘤組織NLRP3/caspase-1/GSDMD表達(dá)升高(圖8)。
核心結(jié)論:氫氣通過誘導(dǎo)焦亡抑制子宮內(nèi)膜癌生長,為臨床治療提供新策略。
2. 研究目的
1.驗證氫氣能否激活 焦亡通路(NLRP3/caspase-1/GSDMD)抑制子宮內(nèi)膜癌。
2.闡明氫氣誘導(dǎo)焦亡的 分子機制(ROS依賴性)。
3.評估富氫水在 動物模型 中的抗腫瘤效果。
3. 研究思路
1.臨床樣本分析:
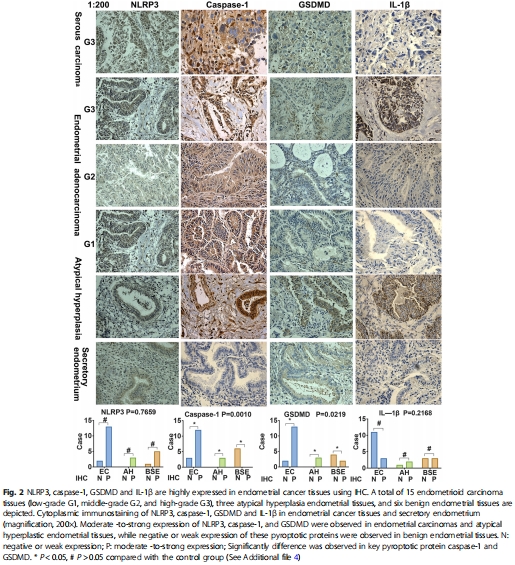
免疫組化(IHC)檢測人子宮內(nèi)膜癌組織中NLRP3、caspase-1、GSDMD表達(dá)(圖2)。
2.體外機制驗證:
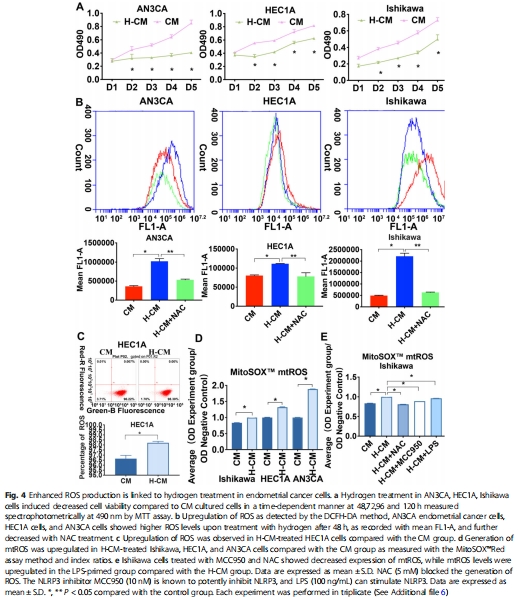
氫氣處理:Western blot分析焦亡蛋白表達(dá)(圖3);DCFH-DA/MitoSOX檢測ROS(圖4b-d)。
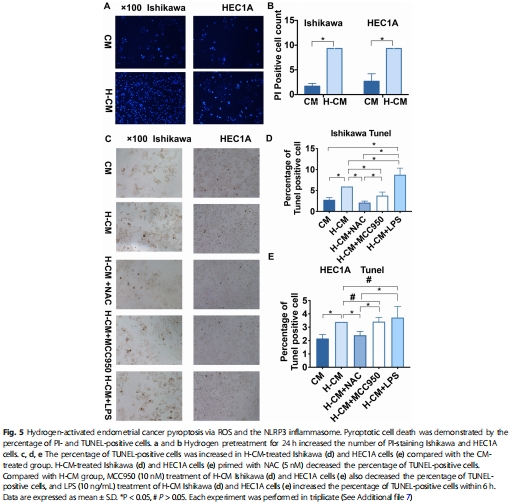
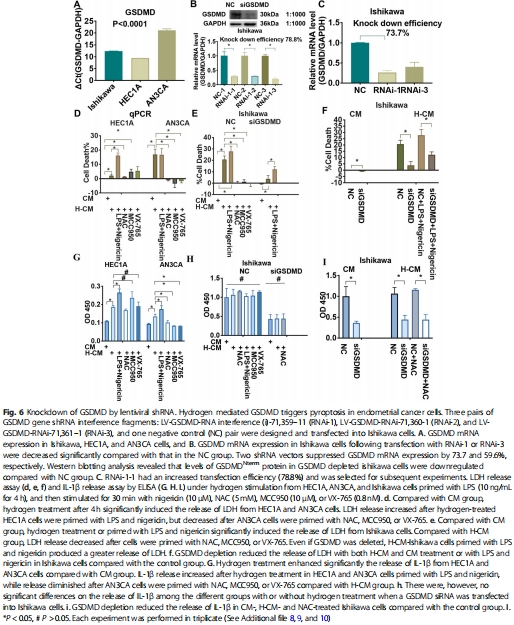
功能實驗:PI/TUNEL染色(圖5)、LDH/IL-1β釋放(圖6)、GSDMD敲低(圖6a-c)。
3.體內(nèi)療效評估:
構(gòu)建人源腫瘤異種移植(PDX)小鼠模型,富氫水干預(yù)(圖7)。
活體成像監(jiān)測腫瘤生長(圖7d-e),IHC分析腫瘤組織焦亡蛋白(圖8)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
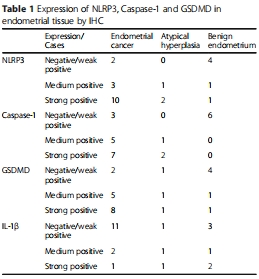
(1) 焦亡蛋白在子宮內(nèi)膜癌中高表達(dá)(圖2, 表1)
數(shù)據(jù):
IHC顯示86.7%癌組織高表達(dá)NLRP3/GSDMD,80%高表達(dá)caspase-1(vs. 正常組織)。
意義:首次證實子宮內(nèi)膜癌存在焦亡現(xiàn)象,為靶向治療提供依據(jù)。
(2) 氫氣激活ROS-焦亡通路(圖3-4)
數(shù)據(jù):
Western blot:氫氣處理上調(diào)NLRP3、ASC、caspase-1、GSDMDNterm(圖3a-c)。
ROS檢測:氫氣顯著增加細(xì)胞內(nèi)ROS(DCFH-DA)和線粒體ROS(MitoSOX)(圖4b-d)。
意義:揭示氫氣通過ROS-NLRP3軸觸發(fā)焦亡的核心機制。
(3) 焦亡表型驗證(圖5-6)
數(shù)據(jù):
PI/TUNEL陽性細(xì)胞增加(圖5a-e),LDH/IL-1β釋放升高(圖6d-i)。
GSDMD敲低后焦亡被抑制(圖6f,i)。
意義:明確GSDMD是焦亡執(zhí)行者,氫氣通過其介導(dǎo)細(xì)胞裂解。
(4) 體內(nèi)抗腫瘤效果(圖7-8)
數(shù)據(jù):
富氫水組小鼠腫瘤體積減小(圖7a-b),活體成像顯示輻射強度(ROI)降低(圖7d-e)。
腫瘤組織NLRP3/caspase-1/GSDMD表達(dá)增強(圖8)。
意義:富氫水通過焦亡通路抑制腫瘤生長,具臨床轉(zhuǎn)化潛力。
5. 結(jié)論
1.氫氣誘導(dǎo)焦亡:通過ROS/NLRP3/caspase-1/GSDMD通路觸發(fā)子宮內(nèi)膜癌細(xì)胞焦亡。
2.體內(nèi)有效性:富氫水顯著抑制小鼠移植瘤生長,伴隨焦亡蛋白表達(dá)升高。
3.治療潛力:氫氣為子宮內(nèi)膜癌提供了一種安全、新型的治療策略。
6. 丹麥Unisense電極的核心價值
(1) 技術(shù)應(yīng)用背景
精確控氫:使用Unisense H?微傳感器(檢測限0.3 μM)實時監(jiān)測溶解氫濃度(方法部分)。
關(guān)鍵作用:確保體外實驗中氫氣處理濃度準(zhǔn)確(H-CM中溶解氫濃度0.7 mM),為機制研究提供 可重復(fù)的氫氣暴露條件。
(2) 科學(xué)意義
排除濃度偏差:Unisense數(shù)據(jù)證實氫氣處理濃度的一致性(圖未直接展示,但為所有體外實驗基礎(chǔ)),避免因濃度波動導(dǎo)致的結(jié)論偏差。
支持機制可靠性:精確的氫氣濃度控制是ROS累積(圖4)和焦亡激活(圖5-6)的前提,保障后續(xù)分子機制數(shù)據(jù)的可信度。
(3) 研究啟示
技術(shù)必要性:在氫氣醫(yī)學(xué)研究中,Unisense電極的 高靈敏度 與 實時監(jiān)測能力 是連接氣體處理與細(xì)胞響應(yīng)的關(guān)鍵工具。
標(biāo)準(zhǔn)化價值:為氫氣治療研究設(shè)立濃度控制金標(biāo)準(zhǔn),推動結(jié)果跨平臺可比性。
總結(jié)
本研究通過 Unisense電極的精準(zhǔn)氫濃度監(jiān)測,結(jié)合多尺度實驗,首次揭示氫氣通過激活焦亡通路抑制子宮內(nèi)膜癌的機制。其技術(shù)貢獻在于:
1.機制可信度保障:Unisense確保氫氣處理濃度精確可控,為ROS-焦亡通路激活提供基礎(chǔ)。
2.轉(zhuǎn)化醫(yī)學(xué)意義:富氫水在動物模型中的有效性(圖7)為臨床氫氣治療子宮內(nèi)膜癌奠定實驗基礎(chǔ)。
3.方法論示范:Unisense在氣體治療研究中的成功應(yīng)用,為類似研究提供技術(shù)范本。
這一工作不僅拓展了氫氣抗癌的機制認(rèn)知,也為子宮內(nèi)膜癌治療提供了新思路。