熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Endogenous brain-sparing responses in brain pH and PO2 in a rodent model of birth asphyxia
在出生窒息的嚙齒動物模型中,腦pH值和PO2的內源性腦保留反應
來源:Acta Physiologica. 2020;229:e13467.
1. 論文摘要核心內容
研究通過建立嚙齒動物(大鼠和豚鼠)新生兒窒息模型,模擬出生窒息(缺氧+高碳酸血癥),探究大腦pH和氧分壓(PO?)的動態變化及內源性保護機制。核心發現:
高碳酸血癥(20% CO?)能恢復窒息期間的腦PO?,并減輕代謝性酸中毒對腦組織的損傷。
單純缺氧(5% O?)導致腦組織堿中毒,與窒息的生理反應截然不同,質疑傳統缺氧模型的臨床相關性。
分級恢復常碳酸血癥(GRN) 可延長窒息后腦PO?超射(overshoot),延緩pH恢復,可能增強神經保護。
結論:高碳酸血癥是窒息時維持腦氧合的關鍵,而GRN策略有望優化新生兒窒息復蘇方案。
2. 研究目的
揭示窒息(缺氧+高碳酸血癥)與單純缺氧對腦組織pH和PO?的影響差異。
闡明高碳酸血癥在腦保護中的作用機制(如調節腦血流、酸堿平衡)。
評估分級恢復常碳酸血癥(GRN) 作為潛在治療策略的可行性。
3. 研究思路
1.模型建立:
使用6日齡(P6)和11日齡(P11)大鼠(模擬早產/足月嬰兒)及新生豚鼠(模擬更成熟腦)。
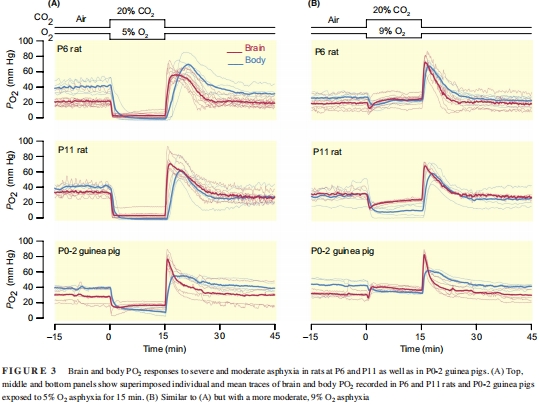
通過吸入低氧(5%或9% O?)+高碳酸(20% CO?)混合氣體驗證窒息效應(圖1-3)。


2.干預設計:
對比窒息(5% O?+20% CO?)、單純缺氧(5% O?)、單純高碳酸(20% CO?)的效應。
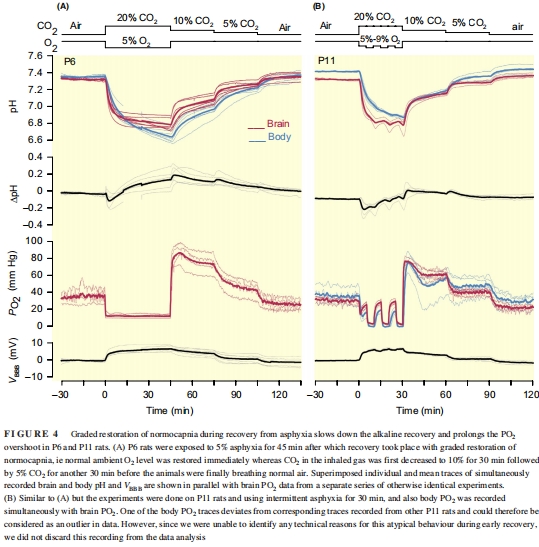
測試GRN策略(窒息后逐步降低CO?濃度)對恢復期的影響(圖4)。
3.多維度監測:
丹麥Unisense微電極實時測量腦/皮下組織pH和PO?(方法部分)。
同步記錄血腦屏障電位(V<sub>BBB</sub>) 和血乳酸水平(驗證代謝性酸中毒)。
4. 關鍵數據及研究意義
(1) pH動態變化(圖1)
數據:
窒息導致腦pH快速下降0.47單位(呼吸性酸中毒),隨后緩慢下降0.10單位(代謝性酸中毒)(圖1A)。
單純缺氧(5% O?)引發腦組織堿中毒(pH↑0.13),而皮下組織酸中毒(圖1C)。
意義:揭示窒息與單純缺氧的生理差異,強調高碳酸血癥對腦pH調節的關鍵作用。
(2) PO?響應(圖2-3)
數據:
9% O?窒息時,腦PO?迅速恢復至基線甚至更高(大鼠P6/豚鼠),而皮下PO?持續低下(圖2B, 3B)。
5% O?缺氧時,腦/皮下PO?均降至近零(圖1C, 3A)。
意義:證實高碳酸血癥通過擴張腦血管維持腦氧合,體現“腦保護效應”。
(3) GRN效應(圖4)
數據:
GRN(逐步降CO?)延長窒息后腦PO?超射(峰值達基線3倍),并延緩pH恢復(圖4A-B)。
意義:支持GRN作為潛在治療策略,通過延長高氧窗口增強神經保護。
(4) 血腦屏障電位(V<sub>BBB</sub>)
數據:V<sub>BBB</sub>變化與pH同步,無破裂跡象(方法部分)。
意義:提示BBB完整性未受窒息破壞,為無創監測提供依據。
5. 丹麥Unisense電極數據的核心價值
(1) 技術優勢
超高時空分辨率:
腦組織pH電極(25μm)、PO?電極(10μm)實現細胞微環境實時監測(方法部分)。
雙區同步對比:同步記錄腦與皮下組織數據,揭示腦特異性保護機制(如代謝性酸中毒在腦中更輕)。
(2) 顛覆性發現
1.窒息 vs. 缺氧的本質差異:
Unisense數據首次證實:
單純缺氧引發腦堿中毒(傳統模型忽略高碳酸的作用)。
窒息時高碳酸恢復腦PO?(圖3B)。
→ 質疑單純缺氧模型的臨床相關性,推動窒息研究范式轉變。
2.GRN的神經保護機制:
PO?超射延長(圖4)表明GRN可能通過維持高氧狀態減少再灌注損傷。
pH緩慢恢復提示延緩堿中毒可抑制神經元過度興奮(減少癲癇風險)。
(3) 臨床轉化意義
診斷價值:腦PO?/pH實時監測可優化新生兒窒息評估(優于血乳酸或血氣)。
治療指導:支持臨床探索GRN策略(如逐步降低通氣CO?),避免快速復氧損傷。
技術延伸:為無創腦監測(如DC-EEG記錄V<sub>BBB</sub>)提供理論依據。
6. 研究結論
1.高碳酸血癥是核心保護機制:20% CO?通過擴張腦血管維持腦PO?,減輕代謝性酸中毒。
2.單純缺氧不模擬窒息:缺氧引發腦堿中毒,與窒息病理生理無關。
3.GRN的潛在價值:逐步恢復常碳酸血癥可延長腦高氧窗口,延緩pH恢復,抑制癲癇活動。
4.模型革新意義:強調未來新生兒窒息研究需整合缺氧+高碳酸雙因素。
7. 核心圖示:內源性腦保護機制
窒息時高碳酸血癥的作用:
[缺氧] + [高碳酸] → [腦血管擴張] → [腦PO?恢復]
↑
[呼吸性酸中毒] → [抑制神經元興奮性]
↓
[代謝性酸中毒減輕] → [減少腦損傷]
GRN延長保護窗口:
[逐步降CO?] → [延長PO?超射] + [延緩pH恢復] → [抑制再灌注損傷]
Unisense電極研究的啟示:
丹麥Unisense微電極通過實時、原位監測腦組織微環境,揭示了窒息中高碳酸血癥的神經保護機制,為新生兒窒息提供了全新監測指標(腦PO?/pH)和治療靶點(GRN)。未來研究需結合動態腦血流監測,優化窒息復蘇的精準干預策略。