熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Hypoxia-induced hypotension elicits adenosine-dependent phrenic longterm facilitation after arotid denervation
頸動脈去神經術后缺氧引起的低血壓會引起腺苷依賴性膈長期促進
來源:Experimental Neurology 333 (2020) 113429
1. 論文摘要核心內容
研究揭示了頸動脈去神經化(CBX)后低氧誘導的低血壓通過腺苷依賴機制引發膈肌長期促進效應(pLTF):
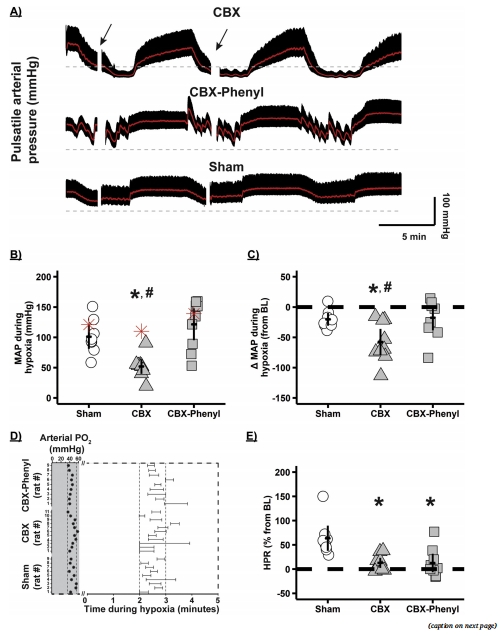
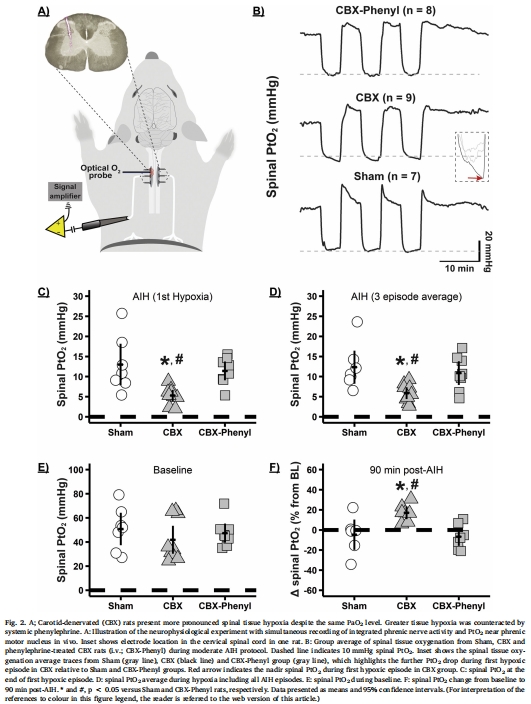
頸動脈去神經化(CBX)大鼠在急性間歇性低氧(AIH)期間出現更嚴重的低血壓(圖1B-C),導致脊髓組織缺氧(圖2B-D)。

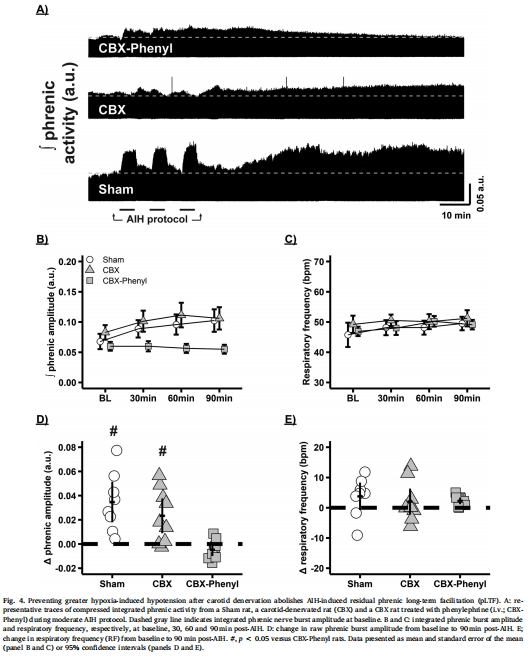
使用苯腎上腺素(Phenylephrine)預防低血壓可消除脊髓缺氧和殘余pLTF(圖4D)。
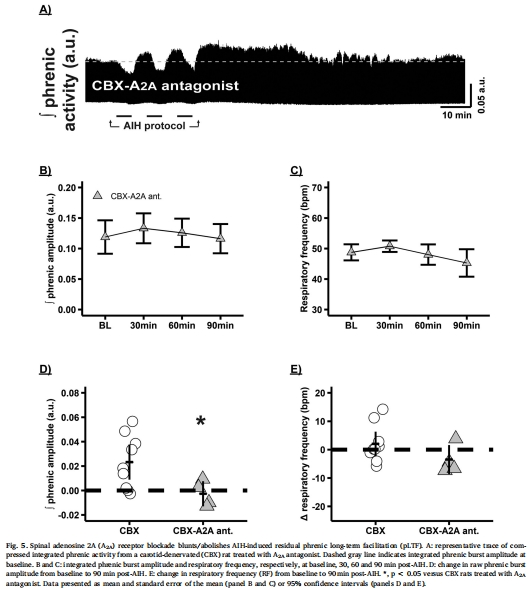
脊髓腺苷A2A受體(而非血清素受體)是殘余pLTF的關鍵介質(圖5D)。
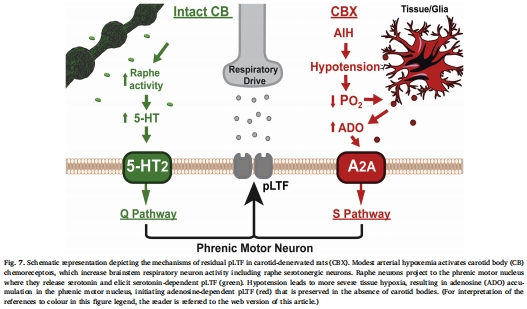
核心結論:CBX后低血壓加重脊髓缺氧,觸發腺苷積累,通過A2A受體通路誘導pLTF(圖7)。
2. 研究目的
探究頸動脈去神經化(CBX)后殘余pLTF的機制,驗證假說:
低血壓→脊髓缺氧→腺苷積累→A2A受體激活→pLTF
旨在闡明循環系統(血壓)與呼吸神經可塑性的耦合機制。
3. 研究思路
1.動物模型:
三組大鼠:假手術組(Sham)、頸動脈去神經組(CBX)、CBX+苯腎上腺素組(CBX-Phenyl)。
中度AIH處理(PaO?: 35-55 mmHg)。
2.關鍵干預:
苯腎上腺素靜脈注射(防止低血壓)。
脊髓注射A2A受體拮抗劑(MSX-3)或5-HT?受體拮抗劑(Ketanserin)。
3.多維度測量:
循環系統:動脈血壓(圖1)、血氣參數(表1-3)。
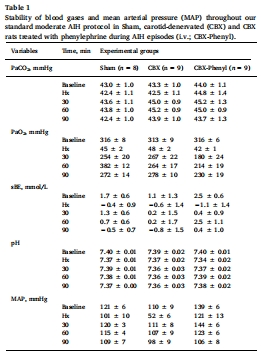
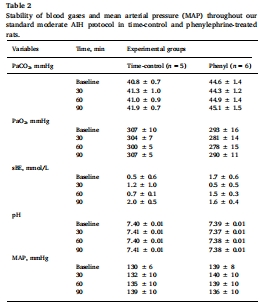
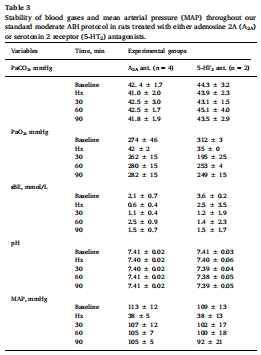
脊髓微環境:組織氧分壓(PtO?,Unisense電極實時監測,圖2-3)。
呼吸輸出:膈神經活動幅度(pLTF,圖4-5)。
4. 關鍵數據及研究意義
(1) 低血壓與脊髓缺氧(圖2)
數據:CBX組AIH期間平均動脈壓(MAP)降至52±6 mmHg(vs. Sham組101±10 mmHg),脊髓PtO?顯著降低(圖2C)。
意義:首次證實低血壓直接導致脊髓缺氧,為腺苷積累提供微環境證據。
(2) 苯腎上腺素的保護作用(圖4)
數據:CBX-Phenyl組MAP維持121±13 mmHg,脊髓PtO?改善,殘余pLTF消失(△幅度:-0.005±0.003 a.u.)。
意義:血壓穩定可預防脊髓缺氧,消除腺苷依賴的pLTF,證明低血壓是核心觸發因素。
(3) A2A受體的關鍵角色(圖5)
數據:脊髓注射A2A拮抗劑(MSX-3)完全阻斷殘余pLTF(p=0.015 vs. CBX組),而5-HT?拮抗劑無效。
意義:確立腺苷(非血清素)通路在CBX后pLTF中的主導地位,顛覆傳統認知。
(4) 血氣參數穩定性(表1-3)
數據:PaO?、PaCO?、pH在組間無差異(表1),排除血氣混雜影響。
意義:確保低血壓是獨立變量,結論聚焦于循環-神經耦聯機制。
5. 丹麥Unisense電極數據的核心意義
(1) 技術創新性
原位實時監測:50μm光學傳感器直接植入頸髓(C3-C4),動態記錄PtO?(圖2A)。
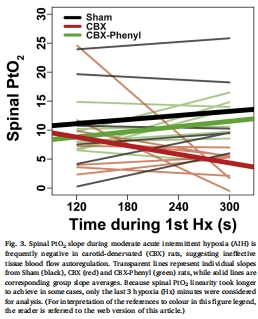
高時空分辨率:1Hz采樣率捕捉AIH期間PtO?瞬態變化(圖2B),發現CBX組PtO?斜率顯著為負(-1.31±0.60 mmHg/min,圖3),提示血流調節障礙。
(2) 科學意義
1.量化組織缺氧:
CBX組PtO?降至<5 mmHg(圖2B),為"腺苷積累閾值"提供直接證據。
苯腎上腺素使PtO?回升至接近Sham組水平(圖2C),確立血壓-氧輸送因果鏈。
2.揭示病理機制:
低血壓導致脊髓毛細血管塌陷,O?釋放受阻(圖7),Unisense數據首次在體驗證該假說。
3.驅動理論革新:
傳統認為pLTF依賴血清素通路,Unisense數據證明在CBX條件下,缺氧-腺苷通路占主導(圖5),重塑呼吸可塑性理論框架。
(3) 轉化價值
臨床啟示:脊髓損傷患者常伴低血壓,Unisense技術可指導AIH治療方案優化(如聯合升壓藥)。
技術標桿:為微環境缺氧研究設立金標準,未來可拓展至腦缺血、腫瘤缺氧等領域。
6. 研究結論
1.機制閉環:CBX→低血壓→脊髓缺氧→腺苷積累→A2A激活→pLTF。
2.通路特異性:殘余pLTF完全依賴腺苷而非血清素通路。
3.治療啟示:血壓管理是保留AIH治療效益的關鍵(如脊髓損傷康復)。