熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Nanocapsule-mediated sustained H2 release in the gut ameliorates metabolic dysfunction-associated fatty liver disease
納米膠囊介導的腸道持續 H 2 釋放可改善代謝功能障礙相關的脂肪肝疾病
來源:Biomaterials 276 (2021) 121030
1. 摘要核心內容
本研究開發了一種新型氨硼烷@中空介孔二氧化硅@PEG納米膠囊(AB@hMSN@PEG),通過封裝氨硼烷(AB)實現腸道靶向、酸響應性緩釋氫氣。該納米膠囊的氫氣負載量相當于3.9 L富氫水(HRW),顯著提升氫氣遞送效率。在飲食誘導肥胖(DIO)和db/db糖尿病小鼠模型中,口服納米膠囊:
減輕代謝功能障礙:降低體重增長(圖2A)、脂肪組織重量(圖2C)、空腹血糖(圖2H)及胰島素抵抗(圖2I-J);
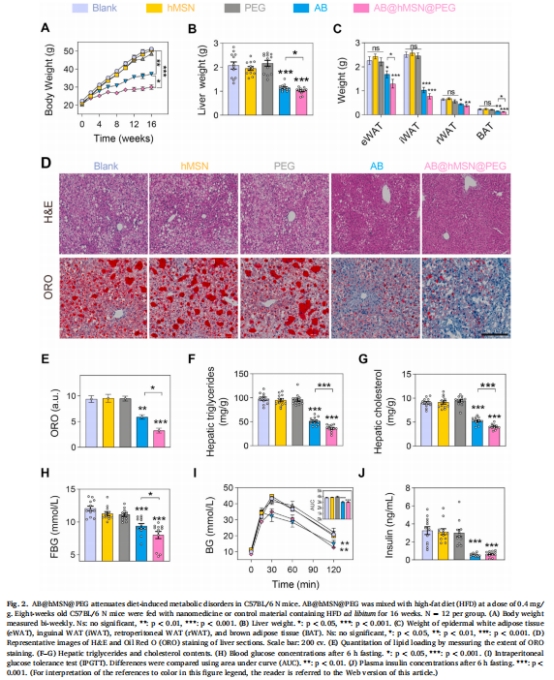
改善早期MAFLD:減少肝臟脂質沉積(圖2E-G)、血漿膽固醇及肝損傷標志物(ALT/AST);
調節腸道菌群:增加益生菌Akkermansia muciniphila豐度(圖4F),并通過菌群依賴與非依賴雙通路改善糖脂代謝。
2. 研究目的
解決當前氫氣療法劑量低、持續時間短的瓶頸問題:
克服富氫水(HRW)遞送效率低(1.6 mg H?/L)的局限;
開發安全高效的高劑量氫氣遞送系統,驗證其對MAFLD、肥胖及糖尿病的治療潛力。
3. 研究思路
材料設計→遞送驗證→動物療效→機制解析:
納米膠囊合成:
中空介孔二氧化硅(hMSN)負載氨硼烷(AB),PEG包覆防泄漏(Scheme 1);
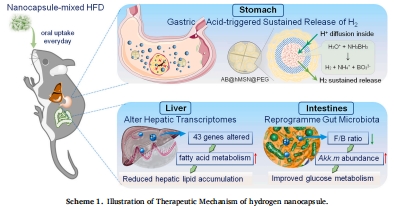
酸響應釋放:胃酸環境(pH 1.2)觸發AB水解產氫(圖1F)。
遞送效率驗證:
體外釋放:Unisense電極實時監測H?釋放動力學(圖1F);
體內分布:微電極動態檢測肝臟H?濃度(圖1G),氣相色譜分析血H?(圖1H)。
動物模型驗證:
DIO模型:高脂飲食(HFD)C57BL/6N小鼠,口服納米膠囊16周(圖2);
db/db模型:遺傳性肥胖糖尿病小鼠,評估降糖減脂效果(圖3)。
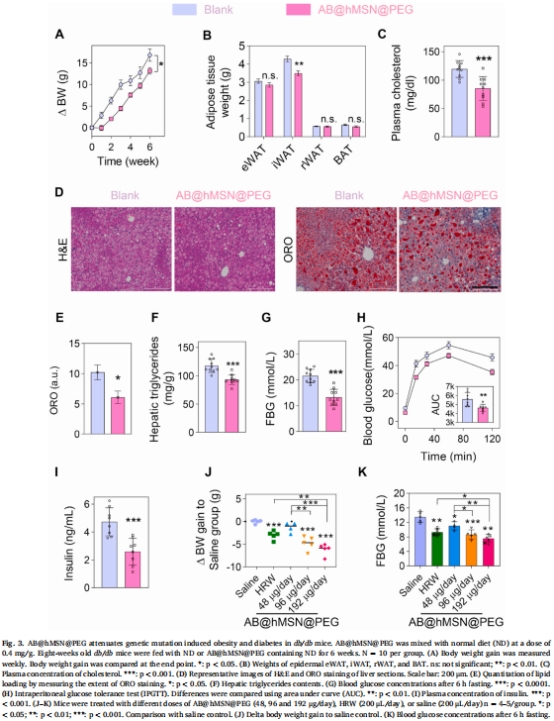
機制探索:
腸道菌群測序:分析Akkermansia等關鍵菌群變化(圖4);
抗生素干預:區分菌群依賴(糖代謝)與非依賴(脂代謝)通路(圖5);
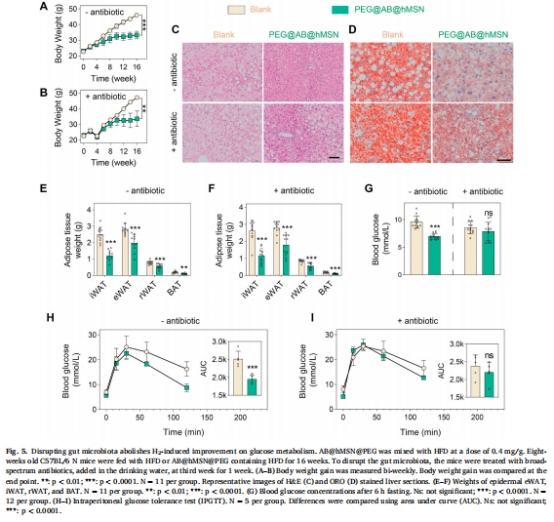
肝臟轉錄組:篩選脂肪酸代謝相關基因(圖6)。
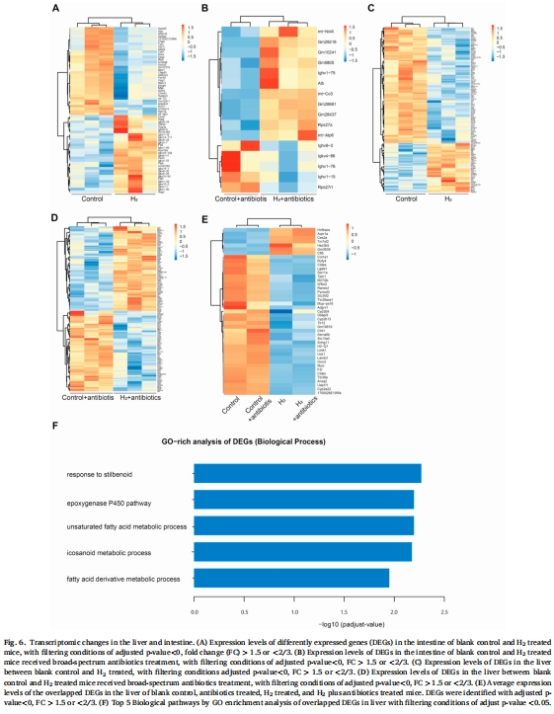
4. 關鍵數據及研究意義
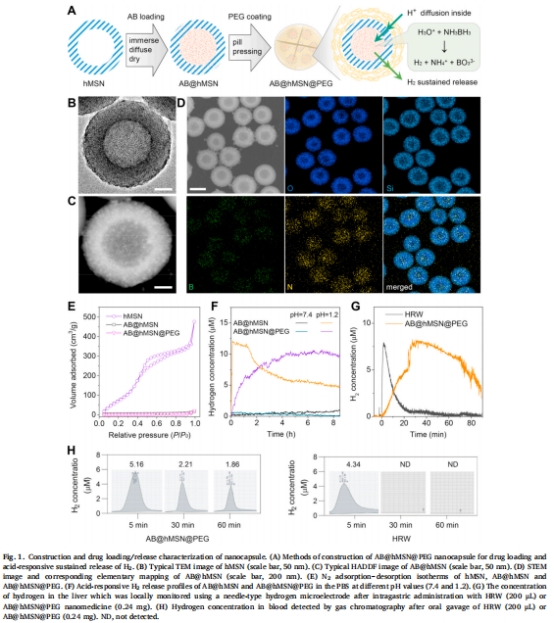
(1)納米膠囊高效遞送氫氣(圖1)
數據:
AB@hMSN@PEG在pH 1.2下持續釋氫>90分鐘(圖1F);
口服后肝臟H?濃度峰值達34 μM(HRW僅6.7 μM),持續時間延長5倍(圖1G)。
意義:首次實現腸道靶向緩釋高劑量H?,突破HRW遞送瓶頸。
(2)顯著改善代謝指標(圖2-3)
數據:
DIO小鼠體重增長減少36.8%(圖2A),肝臟脂質降低40%(圖2G);
db/db小鼠空腹血糖下降50%(圖3G),胰島素水平降低(圖3I)。
意義:證實高劑量H?的量效關系,療效優于臨床藥物二甲雙胍(同等降糖效果)。
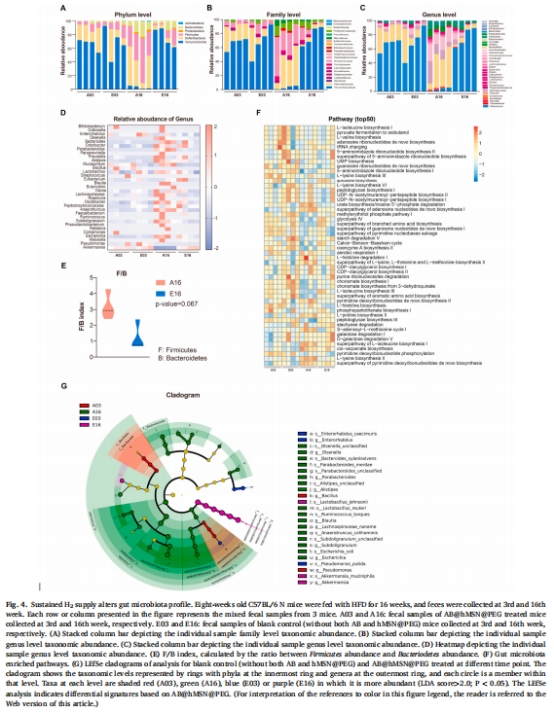
(3)腸道菌群重塑(圖4)
數據:納米膠囊逆轉HFD誘導的Akkermansia muciniphila減少(圖4F),該菌含氫化酶可代謝利用H?。
意義:揭示H?→益生菌增殖→糖代謝改善新通路(圖5G-I)。
(4)肝臟代謝重編程(圖6)
數據:轉錄組顯示脂肪酸氧化基因(如CPT1A)上調,脂合成基因(如SREBP1)下調(圖6F)。
意義:發現菌群非依賴通路——H?直接調控肝臟脂代謝基因,獨立改善MAFLD。
5. 核心結論
材料創新性:AB@hMSN@PEG實現口服高劑量H?緩釋,遞送效率為HRW的5倍。
治療有效性:顯著改善肥胖、糖尿病及早期MAFLD,且無肝腎毒性(補充圖4J)。
雙機制協同:
菌群依賴通路:H?增殖Akkermansia,改善糖代謝(抗生素可阻斷);
直接作用通路:H?重編程肝臟脂代謝基因,獨立改善脂沉積。
臨床潛力:納米膠囊安全(副產物無毒)、成本低,為MAFLD提供新型治療策略。
6. 丹麥Unisense電極的研究意義
技術原理與優勢:
針型微電極(H?-MRCh):直徑100 μm,可植入組織實時監測H?濃度(方法2.6);
高時空分辨率:秒級響應,動態捕捉局部H?釋放動力學(圖1G)。
關鍵科學貢獻:
定量納米膠囊遞送效率:
Unisense數據直接對比HRW與納米膠囊的肝臟H?濃度-時間曲線(圖1G),揭示:
峰值濃度:納米膠囊(34 μM) vs. HRW(6.7 μM);
持續時間:納米膠囊(>90 min) vs. HRW(<15 min);
總暴露量(AUC):納米膠囊為HRW的5.1倍。
驗證酸響應釋放特性:
體外pH 1.2模擬胃酸環境,電極實時記錄H?爆發式釋放(圖1F),支持"腸道靶向"設計。
關聯材料性能與療效:
高劑量長時程的H?暴露(圖1G-H)與顯著代謝改善(圖2-3)形成量效關系,為"高劑量H?增效"假說提供實證。
領域突破性價值:
解決傳統檢測法(氣相色譜)的低時空分辨率缺陷,首次實現活體器官H?藥代動力學動態追蹤;
為納米藥物遞送系統評價提供原位實時監測方法論,推動氫氣治療向精準化發展。