熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Mycobacteria Tolerate Carbon Monoxide by Remodeling Their Respiratory Chain
分枝桿菌通過重塑呼吸鏈來耐受一氧化碳
來源:mSystems May/June 2021 Volume 6 Issue 3 e01292-20
1. 摘要核心內容
本研究揭示了恥垢分枝桿菌(Mycobacterium smegmatis)耐受高濃度一氧化碳(CO)的分子機制:
高CO耐受性:20% CO環境下僅輕微抑制生長(延滯期延長1.3倍),最終生物量與正常條件相當(圖1)。
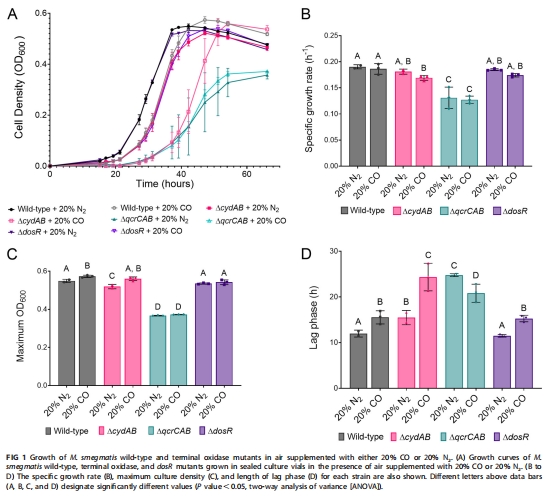
關鍵適應機制:誘導表達細胞色素bd氧化酶(CydAB,24倍上調),其活性對CO不敏感,而細胞色素bcc-aa?氧化酶(QcrCAB)則被CO強烈抑制(圖2, 圖3)。
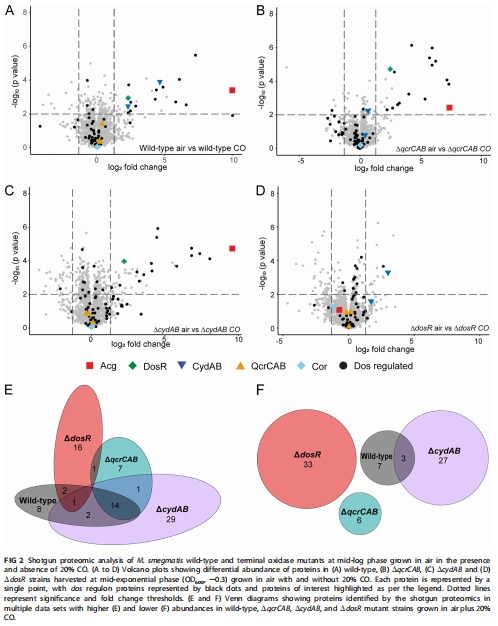
蛋白組學特征:37個差異蛋白(僅占全蛋白組的0.56%),包括部分dos調節子(如DosR上調5倍),但dos調節子缺失(ΔdosR)不影響CO耐受性(圖2)。
呼吸鏈重塑:缺失bd氧化酶的突變株(ΔcydAB)在CO中生長嚴重受損(延滯期延長2.5倍),證明bd氧化酶是CO耐受的核心(圖1, 圖3)。
核心結論:分枝桿菌通過誘導CO不敏感的bd氧化酶重塑呼吸鏈,維持能量代謝,而非依賴廣泛的蛋白組重構。
2. 研究目的
探究分枝桿菌抵抗CO毒性的分子機制,聚焦:
CO對生長和呼吸鏈的影響;
關鍵蛋白(如終端氧化酶、dos調節子)在CO耐受中的作用;
呼吸鏈重塑是否為核心適應策略。
3. 研究思路
多維度驗證模型:
生長表型分析:比較野生型(WT)與突變株(ΔqcrCAB, ΔcydAB, ΔdosR)在20% CO vs. 20% N?下的生長曲線(延滯期、比生長速率、生物量)(圖1)。
蛋白組學:質譜分析CO暴露下WT及突變株的差異蛋白(圖2,表S1),識別關鍵誘導蛋白。
呼吸功能檢測:
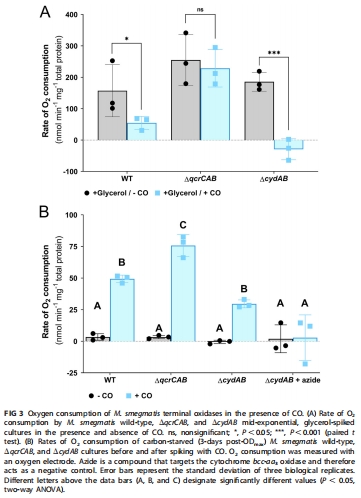
Unisense微電極技術:實時監測O?消耗速率(OCR),評估CO對呼吸鏈的抑制(圖3)。
關鍵實驗:添加甘油(呼吸底物)后注入CO飽和緩沖液,量化呼吸抑制程度。
遺傳驗證:CRISPRi敲低(cydA, qcrC, dosR)與基因缺失突變株表型比對(圖S1)。
4. 測量數據及研究意義
(1)關鍵數據來源與意義
指標 數據來源 研究意義
生長延滯期延長 圖1A,D WT在CO中延滯期↑1.3倍,ΔcydAB突變株↑2.5倍 → bd氧化酶缺失加劇CO敏感性。
蛋白組重塑 圖2A,E bd氧化酶亞基CydA(24倍↑)、CydB(4.8倍↑)及部分dos調節子(如DosR 5倍↑) → 呼吸鏈重構是核心適應策略。
呼吸鏈抑制差異 圖3A CO使ΔcydAB突變株OCR↓100%,WT↓部分,ΔqcrCAB不受抑制 → bd氧化酶具有CO抗性。
CO氧化耦合呼吸 圖3B 碳饑餓時添加CO刺激OCR(ΔqcrCAB↑1.5倍),鋅疊氮化物(細胞色素氧化酶抑制劑)阻斷該效應 → CO可通過bd氧化酶驅動呼吸。
5. 核心結論
呼吸鏈重塑主導CO耐受:
bd氧化酶(CydAB)是關鍵CO不敏感終端氧化酶,其誘導表達補償bcc-aa?氧化酶的CO敏感性。
dos調節子雖被CO誘導,但缺失(ΔdosR)不影響生長耐受(圖1),表明其非核心適應機制。
分枝桿菌固有高抗性:僅0.56%蛋白差異表達 → 表明其代謝網絡對CO脅迫具有強魯棒性。
CO雙面性:
高濃度(20%)抑制敏感氧化酶(bcc-aa?);
低濃度可作為能源(經CO脫氫酶)耦合bd氧化酶維持呼吸(圖3B)。
6. 丹麥Unisense電極(O?微傳感器)的研究意義
技術原理與優勢:
安培法實時監測:電極表面O?還原產生電流信號 → nM級靈敏度 + 秒級分辨率(方法部分)。
原位動態檢測:直接插入細胞懸液,避免采樣偏差 → 精準量化呼吸動力學。
關鍵作用與科學價值:
揭示呼吸鏈抑制差異(圖3A):
直接證明:CO完全抑制ΔcydAB突變株呼吸(依賴bcc-aa?),但僅部分抑制WT(bd氧化酶補償)。
發現:ΔqcrCAB(僅表達bd氧化酶)呼吸完全不受CO影響 → 首次證實bd氧化酶的CO抗性在生理語境有效。
解析CO能源化途徑(圖3B):
監測到碳饑餓時CO添加刺激OCR → 證明CO氧化(經脫氫酶)可向bd氧化酶傳遞電子,驅動呼吸。
鋅疊氮化物抑制實驗:確認該過程依賴終端氧化酶 → 闡明CO代謝與呼吸鏈的耦聯機制。
支撐機制模型:
"Unisense數據揭示:分枝桿菌通過bd氧化酶維持CO環境下的呼吸通量,避免能量崩潰,為耐受性提供直接生理證據。"(討論章節)
領域貢獻:
突破終點法局限 → 實時解析呼吸鏈動態響應;
量化電子傳遞效率 → 為"呼吸鏈重塑"理論提供實驗基石;
技術可推廣至其他氣體脅迫(如NO、H?S)研究。