熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Indium chloride as an electrolyte additive for primary aqueous Mg batteries
氯化銦作為一次水系鎂電池的電解液添加劑
來源:Electrochimica Acta, Volume 373, 2021, Article Number 137916
《電化學學報》第373卷,2021年,文章編號137916
摘要內容:
研究評估了氯化銦(InCl?)作為電解液添加劑對新型Mg-0.15Ca陽極在水系鎂電池中放電性能的影響。關鍵發現包括:
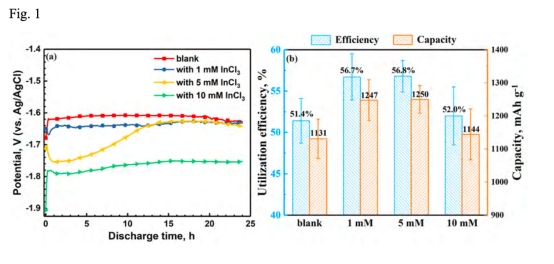
1. 放電電位優化:添加10 mM InCl?使陽極放電電位顯著負移(-1.76 V vs. Ag/AgCl),較空白電解液提升0.15 V(圖1a)。
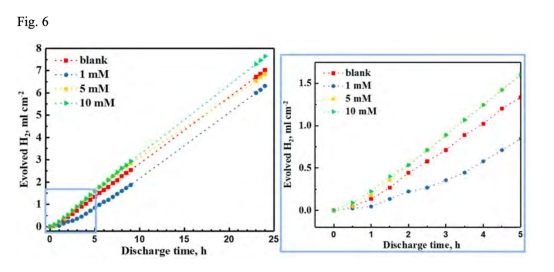
2. 自腐蝕抑制:1 mM InCl?降低自腐蝕速率,但高濃度(10 mM)會加速腐蝕(圖6)。
3. 陽極利用率提升:5 mM InCl?提高陽極利用率至56.8%(空白組51.4%),減少"塊狀效應"(chunk effect)導致的效率損失(圖1b, 7, 8)。
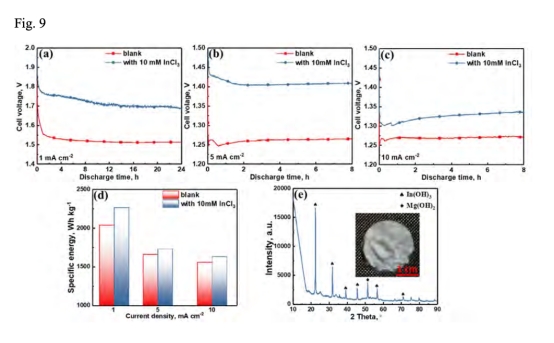
4. 全電池性能:鎂空氣電池在含10 mM InCl?電解液中電壓達1.74 V,比能量2.26 kWh/kg(圖9)。
研究目的:
1. 探究InCl?對Mg-0.15Ca陽極放電電位、自腐蝕速率及利用率的影響機制;
2. 優化InCl?濃度以提升水系鎂電池性能;
3. 揭示In3?水解對局部pH的調控作用及其與放電行為的關聯。
研究思路:
1. 材料制備:
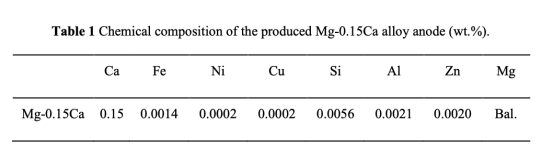
? 陽極:二元Mg-0.15Ca合金(表1);
? 電解液:3.5 wt.% NaCl添加0-10 mM InCl?(pH 3.9-5.6)。
2. 半電池測試:
? 恒流放電(1 mA/cm2)記錄電位與利用率(圖1);
? 實時氫收集量化自腐蝕(圖6)。
3. 表面與界面分析:
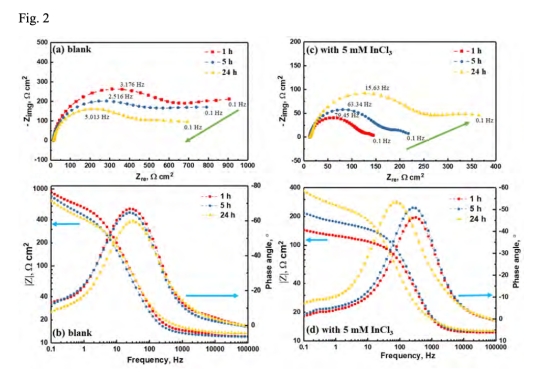
? EIS監測放電過程阻抗變化(圖2);
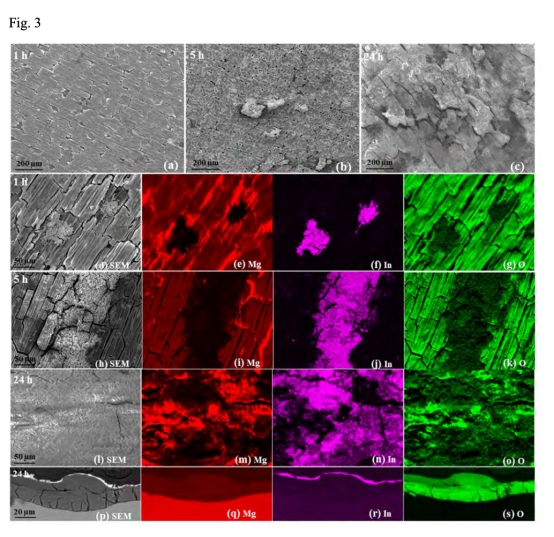
? SEM/EDS表征放電產物形貌與成分(圖3);
? 三維形貌重建分析溶解均勻性(圖8)。
4. 局部pH測量:
? 丹麥Unisense pH微電極(10 μm尖端)實時監測電極/溶液界面pH梯度(圖5)。
5. 全電池驗證:
? 組裝Mg-空氣電池測試放電曲線與比能量(圖9)。
測量數據及其研究意義:
1. 放電電位與利用率(圖1a-b)
? 數據:10 mM InCl?使電位穩定于-1.76 V(vs. Ag/AgCl),利用率56.8%(空白組51.4%)。
? 意義:證實高濃度InCl?通過抑制局部pH升高維持負電位,同時改善溶解均勻性。
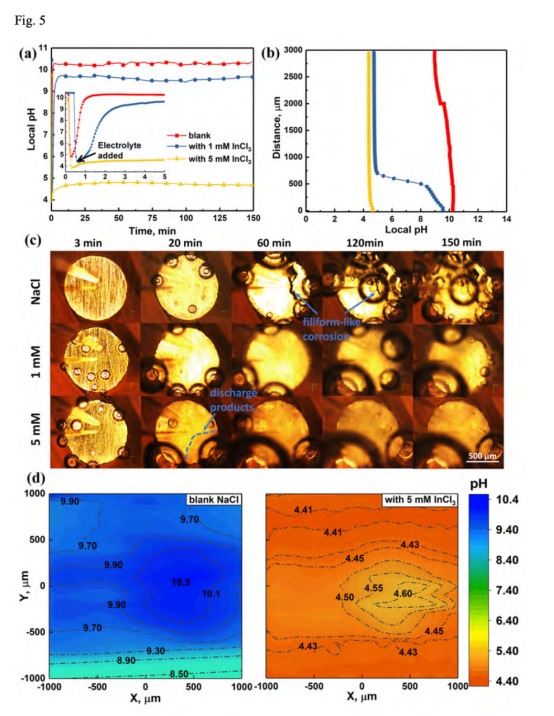
2. 局部pH分布(圖5a-b)
? 數據:Unisense微電極測得20 μm處pH在5 mM InCl?中穩定于4.6(空白組升至10.3)。
? 意義:揭示In3?水解(In3? + H?O → In(OH)? + H?)的pH緩沖效應,解釋放電電位負移機制。
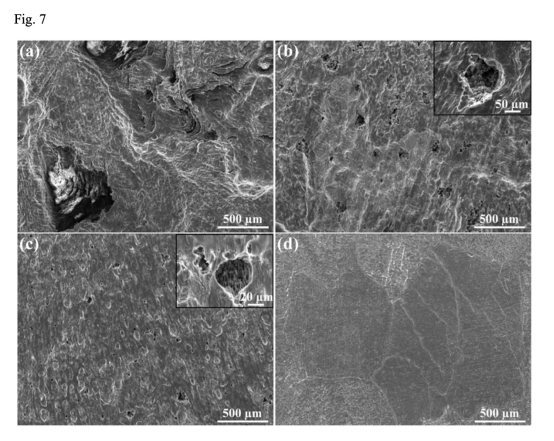
3. 表面形貌與成分(圖3, 7)
? 數據:SEM顯示5 mM InCl?中形成In(OH)?/Mg(OH)?雙層膜(外層富銦),表面孔洞減少(圖7c)。
? 意義:In(OH)?多孔層促進離子傳輸,降低膜電阻(圖2c),同時抑制塊狀脫落。
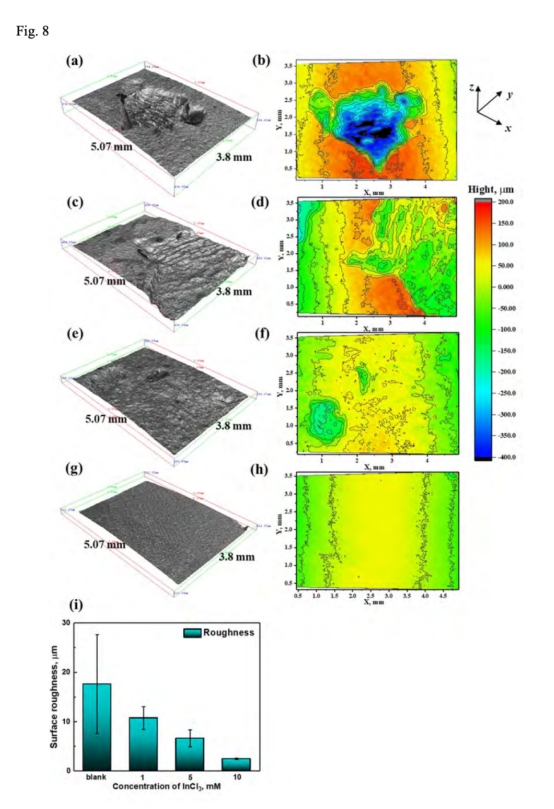
4. 三維粗糙度(圖8i)
? 數據:表面粗糙度隨InCl?濃度增加而降低(10 mM時Ra=15.2 μm,空白組Ra=28.7 μm)。
? 意義:量化溶解均勻性提升,證實InCl?減少"塊狀效應"導致的陽極利用率損失。
5. 全電池性能(圖9a-d)
? 數據:添加10 mM InCl?使電池電壓提升220 mV(1.52 V→1.74 V),比能量達2.26 kWh/kg。
? 意義:驗證InCl?在實際電池體系中的可行性,但陰極沉淀(In(OH)?/Mg(OH)?)需膜分離設計優化。
結論:
1. 濃度依賴性效應:10 mM InCl?最優,使放電電位負移0.15 V,利用率提升5.4%;
2. pH緩沖機制:In3?水解抑制局部pH升高(維持pH~4.6),減少Mg(OH)?鈍化膜形成;
3. 溶解均勻化:In(OH)?沉積層促進均勻溶解,粗糙度降低47%,塊狀效應損失減少4.8%;
4. 應用瓶頸:陰極表面In(OH)?沉淀需通過選擇性滲透膜解決,以維持長期放電穩定性。
丹麥Unisense電極測量數據的研究意義:
使用Unisense pH-10微電極以10 μm分辨率實時監測電極/溶液界面:
1. 空間分辨率優勢:精準定位距電極表面20 μm處的局部pH(圖5a),捕捉到空白電解液中pH從5.6升至10.3,而5 mM InCl?組穩定于4.6,直接驗證In3?水解的pH緩沖機制。
2. 動力學過程解析:實時記錄放電初期pH驟變(圖5a),揭示InCl?在5分鐘內抑制OH?積累的能力,為電位負移提供瞬態證據。
3. 梯度分布測繪:垂直方向pH分布(20-3000 μm)顯示高濃度InCl?組微區與體相pH趨近(圖5b),證明緩沖效應集中于界面。
4. 技術不可替代性:傳統pH探頭無法區分微區與體相差異,而微電極技術為電解液添加劑設計提供了界面化學的直接觀測手段。