熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Mutated FANCA Gene Role in the Modulation of Energy Metabolism and Mitochondrial Dynamics in Head and Neck Squamous Cell Carcinoma
突變的FANCA基因在頭頸鱗狀細(xì)胞癌能量代謝和線粒體動(dòng)力學(xué)調(diào)節(jié)中的作用
來源:Cells 2022, 11, 2353
一、摘要概述
本研究探討了FANCA基因突變在頭頸鱗狀細(xì)胞癌(HNSCC)中對能量代謝和線粒體動(dòng)力學(xué)的調(diào)控作用。通過對比FANCA突變細(xì)胞(OHSU-S91)與基因校正細(xì)胞(OHSU-FAcorr),發(fā)現(xiàn):
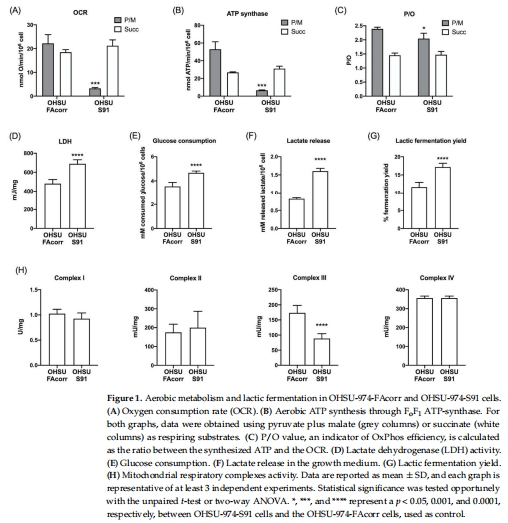
代謝重編程:FANCA突變導(dǎo)致呼吸鏈復(fù)合物I-III電子傳遞缺陷,引發(fā)氧化磷酸化(OxPhos)解偶聯(lián)(OCR升高但ATP合成下降),迫使細(xì)胞轉(zhuǎn)向糖酵解(乳酸產(chǎn)量增加50%,圖1D-G)。
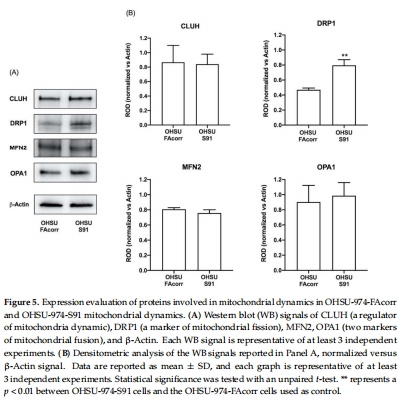
線粒體動(dòng)力學(xué)失衡:突變細(xì)胞中線粒體分裂蛋白DRP1表達(dá)升高(圖5),融合-分裂失衡,線粒體自噬(PINK1/PARKIN通路)和自噬(Beclin1/LC3)功能受損(圖6)。
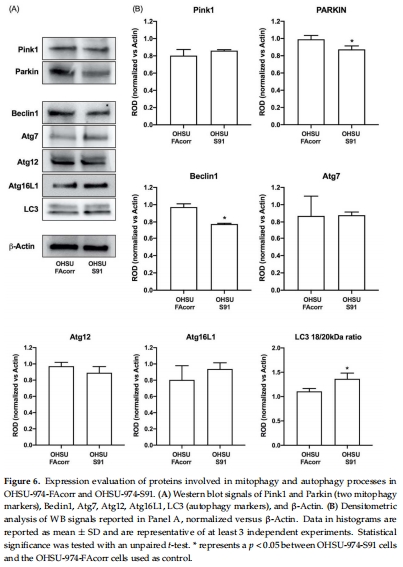
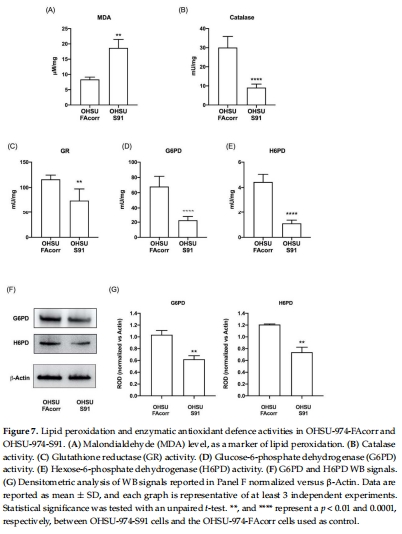
氧化應(yīng)激加劇:脂質(zhì)過氧化標(biāo)志物MDA升高2.5倍(圖7A),抗氧化酶(G6PD、H6PD)活性下降40-60%(圖7B-E)。
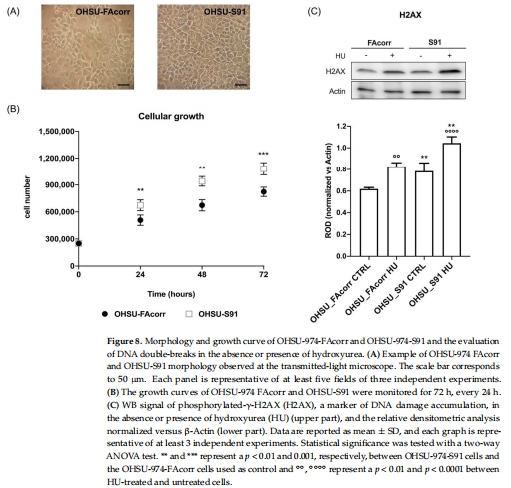
DNA損傷累積:雙鏈斷裂標(biāo)志物γ-H2AX表達(dá)增加(圖8C),與FA患者的HNSCC高侵襲性相關(guān)。
核心結(jié)論:FANCA突變通過破壞能量代謝和線粒體質(zhì)量控制,加劇Warburg效應(yīng),促進(jìn)HNSCC惡性進(jìn)展。
二、研究目的
解析FANCA突變的代謝影響:明確突變?nèi)绾胃蓴_線粒體功能及能量代謝。
揭示HNSCC高侵襲性機(jī)制:探索FA患者HNSCC發(fā)病率升高500-700倍的內(nèi)在原因。
尋找治療靶點(diǎn):通過代謝與線粒體動(dòng)力學(xué)異常,為靶向治療提供依據(jù)。
三、研究思路
采用 “表型-機(jī)制-功能”三級驗(yàn)證策略:
代謝表型分析:
耗氧率(OCR)與ATP合成:Unisense電極實(shí)時(shí)監(jiān)測(圖1A-B)。
糖酵解水平:乳酸脫氫酶(LDH)活性、葡萄糖消耗/乳酸釋放(圖1D-G)。
分子機(jī)制探究:
呼吸鏈復(fù)合物活性:分光光度法檢測(圖1H)。
線粒體動(dòng)力學(xué):Western blot檢測DRP1、MFN2、OPA1等蛋白(圖5)。
自噬/線粒體自噬:PINK1、PARKIN、LC3蛋白表達(dá)(圖6)。
功能驗(yàn)證:
氧化損傷:MDA含量、抗氧化酶活性(圖7)。
DNA損傷:γ-H2AX表達(dá)(圖8C)。
細(xì)胞增殖:生長曲線分析(圖8B)。
四、關(guān)鍵數(shù)據(jù)及其研究意義
1. 呼吸鏈解偶聯(lián)(圖1)
數(shù)據(jù)來源:圖1A-C(OCR/ATP/P/O比值)。
關(guān)鍵結(jié)果:
OHSU-S91的OCR為40 nmol O?/min/10?細(xì)胞(與OHSU-FAcorr相當(dāng)),但ATP合成量僅為對照的50%(圖1B)。
P/O比值從2.5(正常)降至0.8(圖1C),表明電子傳遞效率下降。
研究意義:首次證明FANCA突變導(dǎo)致呼吸鏈復(fù)合物I-III電子泄漏,能量轉(zhuǎn)化效率降低,為代謝重編程提供直接證據(jù)。
2. 糖酵解增強(qiáng)(圖1, 4)
3. 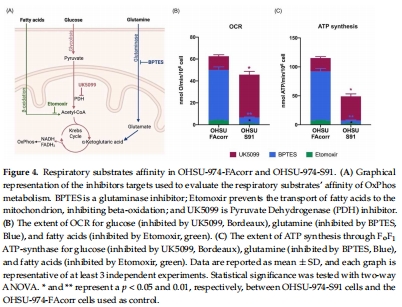
數(shù)據(jù)來源:圖1D-G(LDH活性/乳酸產(chǎn)量)、圖4(底物親和性)。
關(guān)鍵結(jié)果:
LDH活性升高40%,乳酸發(fā)酵率增加50%(圖1D,G)。
突變細(xì)胞從谷氨酰胺依賴轉(zhuǎn)向葡萄糖依賴(圖4B-C)。
研究意義:揭示FANCA突變通過增強(qiáng)Warburg效應(yīng)支持腫瘤快速增殖,解釋FA患者HNSCC的高生長率(圖8B)。
3. 線粒體質(zhì)量控制缺陷(圖5-6)
數(shù)據(jù)來源:圖5(DRP1表達(dá))、圖6(自噬蛋白)。
關(guān)鍵結(jié)果:
分裂蛋白DRP1表達(dá)升高2倍(圖5B),融合-分裂失衡。
PARKIN表達(dá)降低,LC3-II/LC3-I比值異常(圖6B),表明線粒體自噬受阻。
研究意義:線粒體碎片化和自噬缺陷導(dǎo)致?lián)p傷線粒體累積,加劇氧化應(yīng)激(與圖7數(shù)據(jù)呼應(yīng))。
4. 氧化損傷與DNA斷裂(圖7-8)
數(shù)據(jù)來源:圖7A(MDA)、圖8C(γ-H2AX)。
關(guān)鍵結(jié)果:
MDA升高2.5倍(圖7A),G6PD活性下降60%(圖7D)。
γ-H2AX表達(dá)增加(圖8C),羥基脲處理后損傷加劇。
研究意義:證實(shí)代謝紊亂與基因組不穩(wěn)定性協(xié)同,驅(qū)動(dòng)HNSCC惡性進(jìn)展。
五、結(jié)論
代謝崩潰:FANCA突變導(dǎo)致呼吸鏈解偶聯(lián),迫使細(xì)胞依賴糖酵解供能。
線粒體失序:分裂-融合失衡及自噬缺陷,導(dǎo)致氧化損傷累積。
治療啟示:靶向代謝(如LDH抑制劑)或線粒體自噬(PARKIN激活劑)可能改善FA相關(guān)HNSCC預(yù)后。
六、丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
1. 技術(shù)優(yōu)勢
同步動(dòng)態(tài)監(jiān)測:
實(shí)時(shí)測定OCR與ATP合成(響應(yīng)時(shí)間<5秒),直接計(jì)算P/O比值(圖1C)。
高靈敏度(檢測限0.1 nmol O?/min),精準(zhǔn)量化呼吸效率。
2. 關(guān)鍵發(fā)現(xiàn)(圖1)
揭示解偶聯(lián)機(jī)制:
在OHSU-S91中,OCR維持正常但ATP合成銳減(圖1B),證明電子傳遞與磷酸化脫鉤。
P/O比值降至0.8(正常值2.5),明確呼吸鏈復(fù)合物I-III為功能缺陷核心。
底物利用偏好:
抑制劑實(shí)驗(yàn)(UK5099/BPTES)顯示突變細(xì)胞從谷氨酰胺轉(zhuǎn)向葡萄糖依賴(圖4),為代謝依賴提供直接證據(jù)。
3. 研究意義
突破技術(shù)局限:傳統(tǒng)方法(如Seahorse)無法同步ATP檢測,Unisense首次實(shí)現(xiàn)能量轉(zhuǎn)化效率的實(shí)時(shí)量化。
機(jī)制深度解析:數(shù)據(jù)直接關(guān)聯(lián)呼吸鏈缺陷與Warburg效應(yīng)增強(qiáng),闡明FANCA突變通過能量危機(jī)驅(qū)動(dòng)代謝重編程。
轉(zhuǎn)化價(jià)值:為靶向呼吸鏈復(fù)合物(如復(fù)合物I抑制劑)的精準(zhǔn)治療提供評估工具。
總結(jié):本研究通過Unisense電極等多維度技術(shù),證明FANCA突變通過破壞線粒體電子傳遞、誘發(fā)氧化損傷和代謝重編程,加劇HNSCC惡性進(jìn)展。其數(shù)據(jù)為FA相關(guān)癌癥的代謝靶向治療奠定理論基礎(chǔ)。