熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Regulation of Inflammatory Response and Osteogenesis to Citrate-Based Biomaterials through Incorporation of Alkaline Fragments
通過摻入堿性片段調節檸檬酸鹽生物材料的炎癥反應和成骨作用
來源:Adv. Healthcare Mater. 2022, 11, 2101590
一、摘要概述
本文針對檸檬酸鹽基生物材料(如POC)降解過程中釋放檸檬酸導致微環境酸化的問題,設計了一種新型堿性片段BHEp改性的聚檸檬酸酯(POPC)。通過將BHEp引入聚(檸檬酸-1,8-辛二醇)(POC)主鏈,合成POPC聚合物,并與β-磷酸三鈣(β-TCP)復合制備3D打印多孔支架(PTCP)。研究證實:
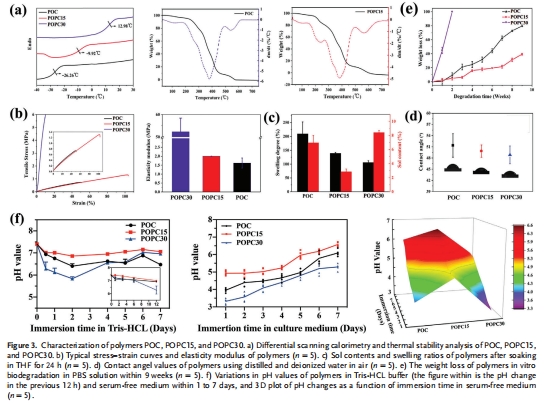
堿性中和作用:BHEp有效中和降解產生的酸性環境(圖3f),將pH穩定在7.0-7.2(生理范圍)。
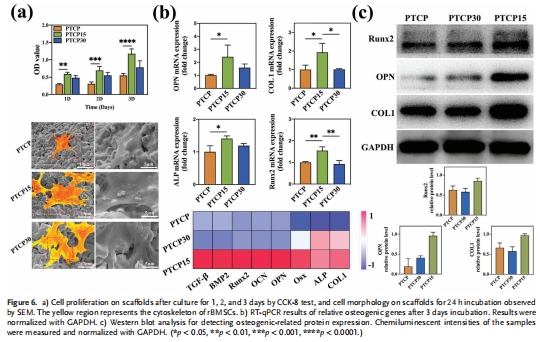
細胞行為改善:POPC15(15% BHEp)顯著促進rBMSCs黏附、增殖及成骨基因表達(圖6b-c),并降低巨噬細胞炎癥反應(圖7e)。
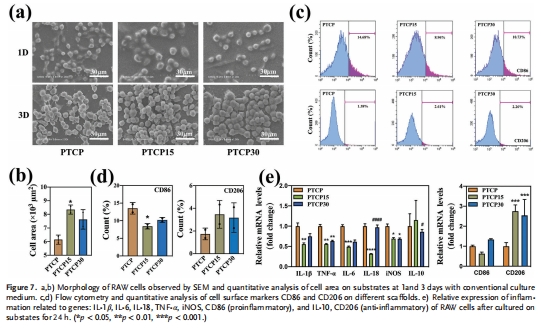
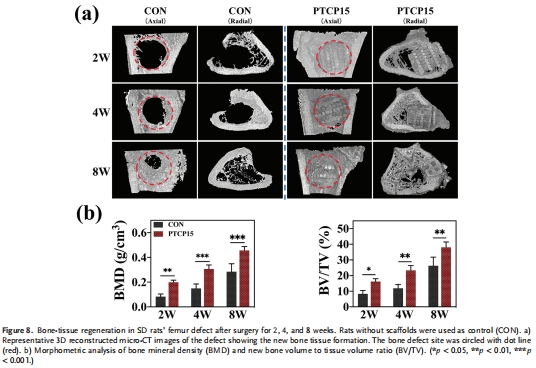
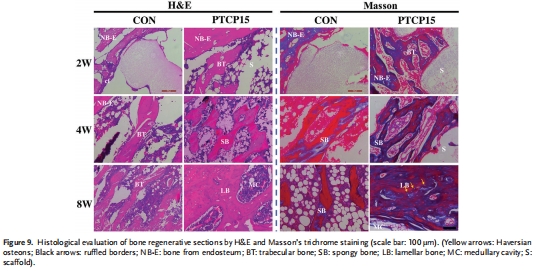
骨再生增強:大鼠股骨缺損模型中,PTCP15支架顯著提升新骨形成(圖8)與骨整合(圖9)。
研究為調控生物材料降解微環境提供了新策略。
二、研究目的
解決降解酸化問題:傳統檸檬酸鹽材料(如POC)降解釋放檸檬酸,導致pH下降(<6.5),抑制細胞活性與骨再生。
優化材料性能:通過引入堿性片段BHEp,中和酸性微環境,改善生物相容性。
驗證骨修復效果:評估POPC/β-TCP支架在體外(細胞響應)和體內(骨缺損修復)的作用機制。
三、研究思路
采用 “材料設計→性能表征→生物學評價→動物驗證” 四步策略:
材料合成:
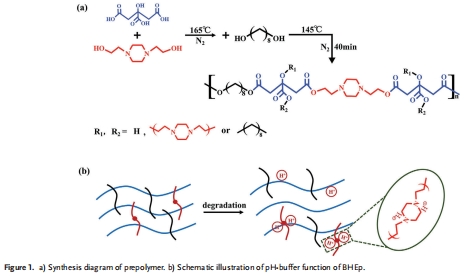
以檸檬酸、1,8-辛二醇和BHEp為單體,通過縮聚反應合成POPC預聚物(圖1a)。
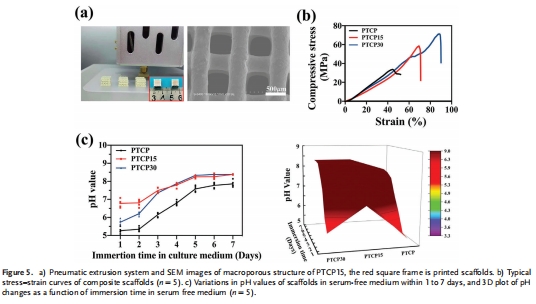
經后聚合得到POPC彈性體,并與β-TCP復合,3D打印多孔支架(圖5a)。
性能表征:
化學結構(FTIR/NMR,圖2a,d)、熱力學性質(DSC/TGA,圖3a)、機械性能(圖3b)、溶脹與降解行為(圖3c,e)。
體外生物學評價:
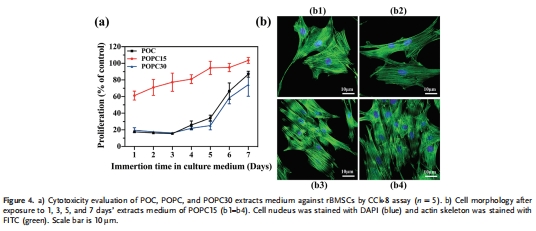
細胞相容性(CCK-8,圖4a)、rBMSCs成骨分化(RT-qPCR/Western blot,圖6)、巨噬細胞炎癥響應(流式細胞術/RT-qPCR,圖7)。
體內骨再生驗證:
大鼠股骨缺損模型,通過Micro-CT(圖8)和組織學(圖9)評估新骨形成。
四、關鍵數據及其研究意義
1. 材料性能數據(圖3)
數據來源:圖3a-f(熱力學、機械、溶脹、降解、pH)。
關鍵結果:
POPC15的pH穩定性最佳(Tris緩沖液中穩定于7.2,圖3f)。
降解9周后POPC15失重僅40%,低于POC的80%(圖3e)。
研究意義:
BHEp通過質子化中和檸檬酸(圖1b),避免pH驟降,為細胞提供適宜微環境。
適度的BHEp含量(15%)平衡了機械強度與降解速率(彈性模量10.46 MPa,圖3b)。
2. 細胞響應數據(圖4, 6, 7)
數據來源:
圖4a(細胞增殖)、圖6b-c(成骨基因/蛋白表達)、圖7e(炎癥基因表達)。
關鍵結果:
rBMSCs在POPC15提取物中增殖率最高(CCK-8,圖4a)。
成骨基因(Runx2, OPN, Col I)表達上調2-3倍(圖6b)。
巨噬細胞促炎基因(IL-1β, TNF-α)下調,抗炎基因(IL-10)上調(圖7e)。
研究意義:
中性pH微環境促進rBMSCs成骨分化,并誘導巨噬細胞向促愈合表型(M2型)極化。
證實材料表面電荷(BHEp質子化后帶正電)增強細胞黏附(接觸角49.5°,圖3d)。
3. 動物實驗數據(圖8, 9)
數據來源:圖8(Micro-CT)、圖9(組織學)。
關鍵結果:
PTCP15組骨礦物密度(BMD)和骨體積分數(BV/TV)顯著高于對照組(*p<0.05,圖8b)。
8周時缺損區形成成熟骨板(哈弗斯系統,圖9)。
研究意義:
堿性微環境協同多孔結構促進血管化骨再生,為臨床骨缺損修復提供新材料。
五、結論
材料創新性:BHEp的引入解決了檸檬酸鹽材料降解酸化的核心問題,POPC15的綜合性能最優。
機制明確:
pH緩沖:BHEp通過質子化中和H?,維持微環境pH>7.0(圖3f)。
免疫調節:降低促炎因子表達,促進巨噬細胞向M2型轉化(圖7c-e)。
應用價值:PTCP15支架顯著增強骨再生(圖8-9),為骨組織工程提供新策略。
六、丹麥Unisense電極數據的詳細解讀
1. 技術優勢
高精度動態監測:
電極尖端直徑10 μm(響應時間1-3秒),實現 微區pH實時追蹤(圖3f, 5c)。
直接輸出絕對pH值(非間接熒光法),避免自發熒光成像的定量偏差。
2. 關鍵數據意義(圖3f, 5c)
降解初期pH調控:
在Tris緩沖液中,POPC15的pH在12小時內從7.0升至7.2,而POC驟降至7.2以下(圖3f)。
證明BHEp的即時中和能力:質子化叔胺基團(R?N + H? → R?NH?)消耗H?。
生理環境驗證:
在無血清培養基中,PTCP15支架維持pH>7.0長達7天(圖5c),克服傳統材料在復雜體液環境的不穩定性。
3. 研究突破
定量關聯材料化學與生物學響應:
Unisense數據直接關聯BHEp含量(15%)與pH穩定性(圖3f),解釋細胞增殖差異(圖4a)。
揭示 “堿性片段→pH緩沖→細胞行為改善” 的因果鏈條(圖1b, 3f, 4a)。
技術不可替代性:
傳統pH試紙或熒光法無法實現秒級動態監測,Unisense電極為降解動力學研究提供關鍵工具。
總結:本研究通過Unisense電極精準量化POPC的pH緩沖能力,證實堿性片段BHEp是調控骨修復微環境的核心要素。其數據不僅解釋了材料降解的化學機制(H?中和),更將材料性能與生物學效應(細胞增殖、成骨分化、炎癥調控)直接關聯,為設計下一代智能骨修復材料奠定基礎。