熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Inoculum Concentration Influences Pseudomonas aeruginosa Phenotype and Biofilm Architecture
接種物濃度影響銅綠假單胞菌表型和生物膜結構
來源:November/December 2022 Volume 10 Issue 6 10.1128/spectrum.03131-22
一、摘要概述
本研究通過藻酸鹽珠生物膜模型探究接種濃度(Inoculum)對銅綠假單胞菌(Pseudomonas aeruginosa)生物表型及生物膜結構的影響:
核心發現:
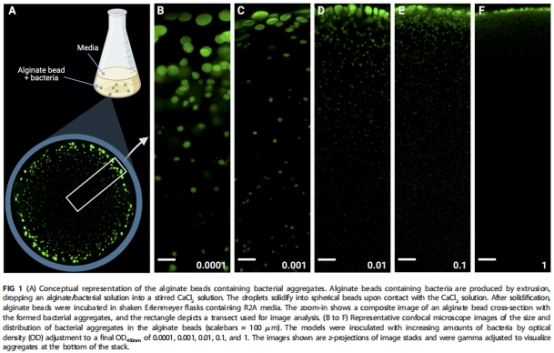
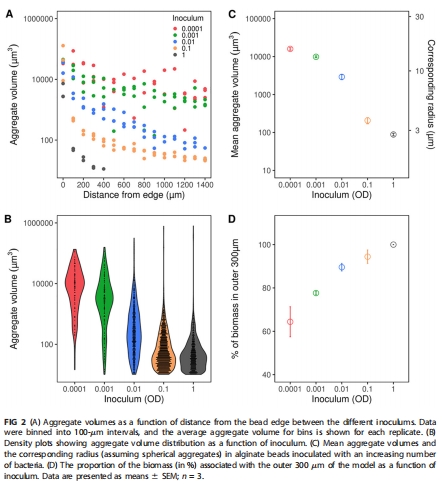
接種濃度顯著改變生物膜聚集體的尺寸與空間分布(圖1B-F)。高接種濃度(OD<sub>450nm</sub>=1)形成密集小聚集體(半徑<6.2μm),低接種濃度(OD<sub>450nm</sub>=0.0001)形成稀疏大聚集體(圖2C)。
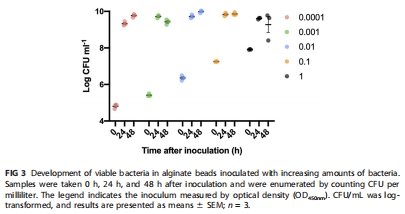
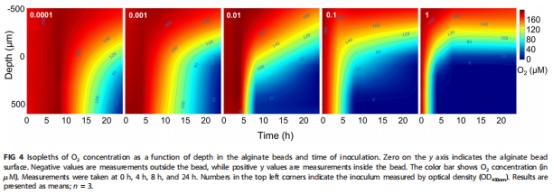
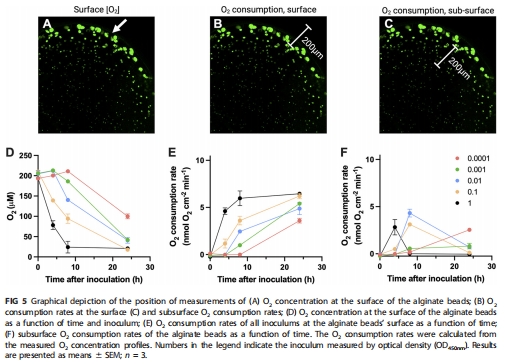
24小時后總生物量無差異(圖3),但微環境氧動態截然不同:高接種組4小時內耗盡內部氧氣(圖4),低接種組維持耗氧至24小時(圖5F)。
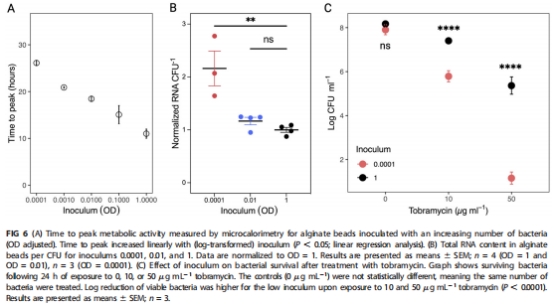
代謝活性與抗生素耐受性相關:高接種組因缺氧進入靜止期,對妥布霉素(Tobramycin)耐受性增強(存活率↑5.37 log CFU/mL)(圖6C)。
二、研究目的
解決兩大科學問題:
驗證接種濃度效應:探究初始細菌密度如何影響生物膜聚集體的形成及微環境(尤其氧氣梯度)。
闡明表型-耐受關聯:揭示微環境變化如何通過代謝活性調控抗生素耐受性。
三、研究思路
采用多尺度動態監測策略:
模型構建:
藻酸鹽珠包埋PAO1-GFP菌株,設置5組接種濃度(OD<sub>450nm</sub>=1至0.0001)(圖1A)。
時空分析:
結構表征:共聚焦顯微鏡(CLSM)量化聚集體尺寸/分布(圖1B-F, 圖2)。
氧動力學:Unisense微電極(Clark型,25μm尖端)實時監測珠內氧濃度剖面(圖4)及耗氧率(圖5)。
代謝活性:微量熱法測熱流峰值時間(圖6A);RNA含量分析(圖6B)。
功能驗證:
妥布霉素處理(10/50 μg/mL),評估存活率與接種濃度的關聯(圖6C)。
四、測量的數據及其研究意義
1. 生物膜結構與分布
數據來源:圖1(CLSM圖像)、圖2(定量分析)。
關鍵結果:
高接種組:聚集體體積小(<1,000 μm3),邊緣密集(生物量占比↑)(圖2D)。
低接種組:聚集體體積大(中心區出現>10,000 μm3聚集體),分布均勻(圖2A)。
研究意義:揭示接種濃度可編程化調控聚集體尺寸,為模擬感染微環境提供新策略。
2. 微環境氧動態
數據來源:圖4(氧等值線)、圖5(耗氧率)。
關鍵結果:
高接種組:4小時內部缺氧,表面耗氧率峰值提前(圖5B,E)。
低接種組:24小時維持耗氧,代謝持續活躍(圖5F)。
研究意義:證實密度依賴的氧擴散限制是微環境異質性的核心驅動力。
3. 代謝與抗生素耐受
數據來源:圖6(熱流/RNA/存活率)。
關鍵結果:
代謝活性:低接種組RNA含量↑2倍,熱流峰值延遲至26小時(圖6A-B)。
抗生素耐受:高接種組妥布霉素存活率↑5.37 log(50 μg/mL)(圖6C)。
研究意義:建立缺氧-代謝停滯-耐受增強的直接因果鏈,解釋生物膜耐藥新機制。
五、結論
核心機制:
接種濃度通過密度依賴的氧競爭塑造生物膜結構:高密度→快速缺氧→小聚集體/靜止期表型→抗生素耐受↑。
技術啟示:
藻酸鹽珠模型可通過調整接種濃度精確模擬感染微環境(如囊性纖維化肺部聚集)。
臨床意義:
體外藥敏試驗需標準化接種濃度,避免因微環境差異誤導療效評估。
六、丹麥Unisense電極數據的詳細解讀
1. 測量原理與技術優勢
工作原理:
Clark型氧電極(OX-25)基于H<sub>2</sub>O<sub>2</sub>電化學還原(O<sub>2</sub> + 4H<sup>+</sup> + 4e<sup>-</sup> → 2H<sub>2</sub>O),電流信號∝氧濃度。
空間分辨率:100 μm步進深度剖面(圖4),時間分辨率:<0.5秒(方法章節)。
校準標準:
雙點校準(空氣飽和水/連二亞硫酸鈉脫氧水),確保μM級精度。
2. 關鍵數據與生物學意義
氧等值線圖(圖4):
高接種組:4小時內部缺氧(藍色區域),證實高密度引發快速氧枯竭。
低接種組:24小時漸進式缺氧,揭示聚集體生長與氧消耗的時空耦合。
耗氧率動力學(圖5):
表面耗氧率(J<sub>O2</sub>)計算:基于Fick定律(公式見方法),顯示高接種組早期峰值(8小時)vs.低接種組持續上升。
科學價值:首次量化接種濃度-耗氧率-代謝停滯的定量關系,為抗生素時機選擇提供依據。
3. 研究意義
技術創新:
實現三維氧梯度原位監測,克服傳統終點法檢測的局限性。
領域貢獻:
揭示微環境氧動態是表型異質性的核心,推動“精準化生物膜模型”構建。
為優化抗生素治療方案(如聯合氧增敏劑)提供理論依據。
總結:本研究通過Unisense微電極等多項技術,證明接種濃度通過調控氧微環境驅動銅綠假單胞菌表型分化,直接影響抗生素療效,為生物膜研究和感染治療提供新視角。