熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
?英文標題:The Effects of Novel Triazolopyrimidine Derivatives on H?S Production in Lung and Vascular Tonus in Aorta
新型三唑并嘧啶衍生物對肺H 2 S生成和主動脈血管緊張的影響
?來源期刊:Pharmacology
?DOI:10.1159/000533419
摘要內容
本研究首次報道了白藜蘆醇(RVT)類似物Cpd2(新型三唑并嘧啶衍生物)對肺組織內源性硫化氫(H?S)生成的促進作用。通過化學合成獲得Cpd1(查爾酮前體)和Cpd2,利用丹麥Unisense微電極實時監測小鼠肺勻漿中H?S動態變化。研究發現:
1.RVT和Cpd2顯著增強L-半胱氨酸誘導的H?S生成(健康肺組織),而Cpd1無效。
2.氧化應激(焦性沒食子酸誘導)顯著抑制肺H?S水平,Cpd2可恢復其至正常水平。
3.H?S合成酶抑制劑(AOAA)完全阻斷Cpd2的促H?S作用,證實其通過內源性H?S合成途徑生效。
4.Cpd1和Cpd2均引起小鼠主動脈濃度依賴性血管舒張,與RVT效果相當。
Cpd2通過增強肺H?S生成并抵抗氧化應激損傷,為呼吸系統疾病(如哮喘、肺動脈高壓)的治療提供了新候選藥物。
研究目的
驗證以下科學假設:
1.RVT及其新型類似物(Cpd1、Cpd2)能否促進肺組織內源性H?S合成。
2.Cpd2能否在氧化應激條件下維持肺H?S水平。
3.新型化合物是否具有血管舒張活性,以評估其對呼吸系統疾病相關血管功能障礙的潛在療效。
研究思路
1.化合物合成與表征:
以3,4-二甲氧基苯甲醛和苯乙酮為原料,經Claisen-Schmidt縮合合成Cpd1(查爾酮結構)。
Cpd1與3-氨基三唑經微波輔助環化反應生成Cpd2(三唑并嘧啶結構),通過NMR、質譜確認結構。
2.H?S生成動力學監測:
提取小鼠肺組織勻漿,加入L-半胱氨酸(H?S合成底物)。
使用Unisense H?S微電極實時檢測H?S濃度變化。
對比健康/氧化應激(焦性沒食子酸處理)條件下RVT、Cpd1、Cpd2的作用。
3.機制驗證:
加入H?S合成抑制劑AOAA,觀察化合物促H?S作用是否被阻斷。
4.血管功能評估:
離體小鼠主動脈環實驗,檢測化合物對苯腎上腺素預收縮血管的舒張效應。
1.H?S生成速率(圖4c):
數據來源:健康肺勻漿中L-半胱氨酸誘導的H?S生成斜率。
意義:Cpd2使H?S生成速率從0.50±0.05μM/min增至0.74±0.04μM/min(p<0.01),證實其顯著促進內源性H?S合成。
2. 最大H?S濃度(圖4b):
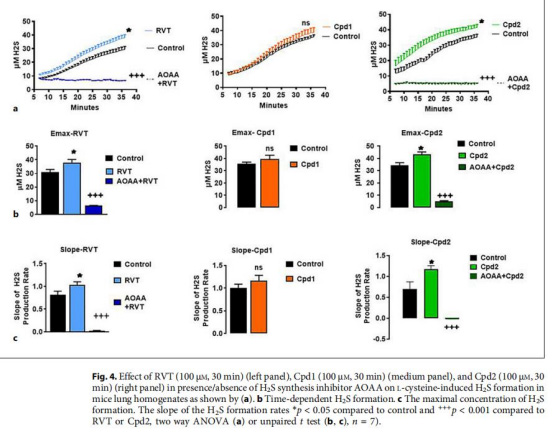
數據來源:肺勻漿中H?S峰值濃度。
意義:Cpd2使H?S濃度從對照34.40±2.04μM升至43.11±2.17μM(p<0.05),效果與RVT相當,且被AOAA完全抑制(→4.87±0.61μM,p<0.001),依賴H?S合成酶途徑。
3. 氧化應激下H?S恢復(圖5b):
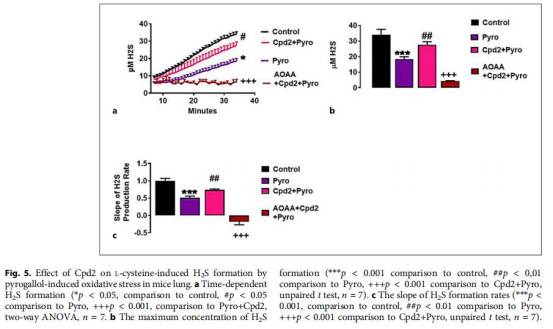
數據來源:焦性沒食子酸處理的肺勻漿H?S峰值。
意義:氧化應激使H?S降至8.40±1.53μM,Cpd2恢復至27.59±1.98μM(p<0.01),凸顯其抗氧化應激損傷潛力。
4. 血管舒張效應(圖7a):
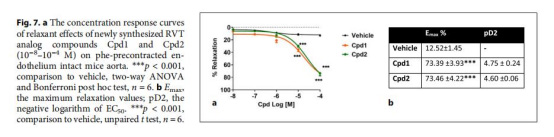
數據來源:主動脈環舒張率(%)。
意義:Cpd1和Cpd2均引起73%血管舒張(p<0.001),提示其改善血管張力的潛力。
丹麥Unisense微電極數據的詳細研究意義
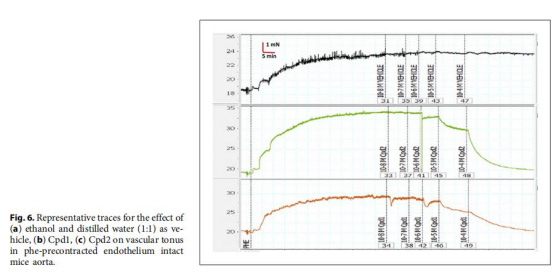
數據來源:圖3-5(H?S實時生成曲線)
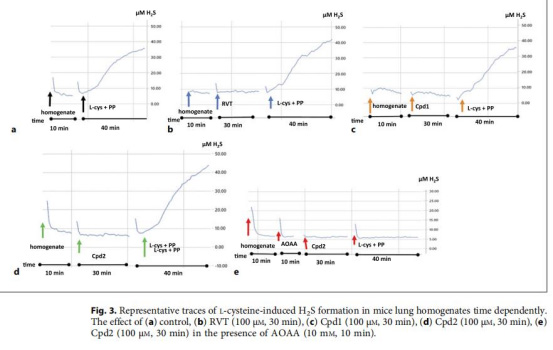
技術原理:Unisense H?S-500LR微電極通過電化學還原反應實時檢測H?S分壓(μM級分辨率),校準曲線基于Na?S標準品(5-80μM)。
核心發現與意義:
1.動態過程解析:
首次捕獲肺勻漿中H?S生成的實時動力學曲線(圖3),揭示Cpd2給藥后H?S持續上升(30分鐘),而Cpd1無效。
2.機制特異性驗證:
AOAA(H?S合成抑制劑)完全阻斷Cpd2的促H?S作用(圖4a),排除化合物自身作為H?S供體的可能性,確認為內源性合成激活。
3.氧化應激響應:
直接量化氧化應激下H?S的快速耗竭(焦性沒食子酸使H?S↓75%)及Cpd2的修復效果(↑230%)(圖5a),為抗氧化-抗炎聯合療法提供依據。
4.技術優勢:
毫秒級時間分辨率:精確測定H?S生成速率(斜率),避免傳統終點法(如亞甲基藍法)的時序信息丟失。
高靈敏度:檢測限低至μM級,適用于微量組織勻漿分析。
結論
1.新型化合物Cpd2作為RVT類似物,首次被證實能顯著促進肺組織內源性H?S生成(↑25%),效果與RVT相當且依賴H?S合成酶途徑。
2.Cpd2能抵抗氧化應激對H?S系統的破壞,恢復耗竭的H?S水平至近正常值,對哮喘、肺動脈高壓等氧化應激相關呼吸疾病具治療潛力。
3.Cpd1和Cpd2均展現強效血管舒張活性(舒張率73%),提示其改善呼吸疾病血管功能障礙的雙重作用。
4.Unisense微電極技術為H?S動力學研究提供高精度方法學支持,推動靶向H?S通路的新型藥物研發。