熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Hydrogen Attenuates Inflammation by Inducing Early M2 Macrophage Polarization in Skin Wound Healing
氫氣通過誘導皮膚傷口愈合中早期 M2 巨噬細胞極化來減輕炎癥
期刊:Pharmaceuticals
年份:2023
DOI:https://doi.org/10.3390/ph16060885
摘要核心內容
本研究通過小鼠背部全層皮膚缺損模型,探究氫氣(H?)吸入對炎癥期傷口愈合的影響。研究發現:
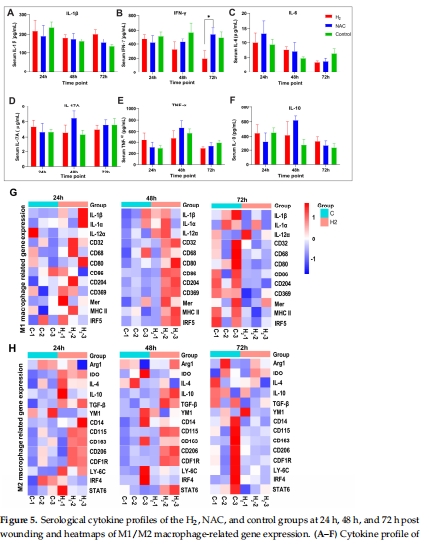
H?促進早期傷口愈合:顯著減少炎癥細胞浸潤,改善傷口床狀態(圖1D-E)。
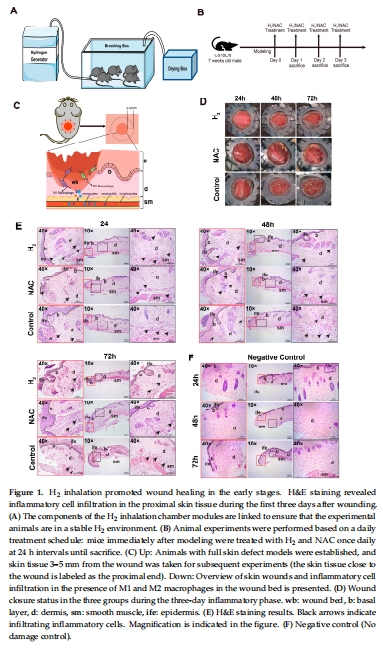
誘導M2巨噬細胞極化:在傷口后第2-3天(比常規愈合提前2-3天)促進M1向M2表型轉化(圖3B-C)。
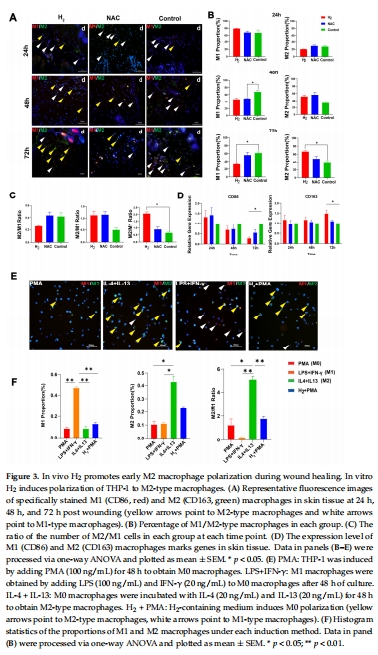
調節炎癥因子:降低血清促炎因子(IL-1β、TNF-α、IL-6),提升抗炎因子IL-10水平(圖5)。
非依賴抗氧化機制:H?的效果優于抗氧化劑NAC,表明其作用超越單純ROS清除(圖3F)。
結論:H?通過早期誘導M2巨噬細胞極化減輕炎癥,為臨床傷口護理提供新策略。
研究目的
驗證H?對巨噬細胞極化的影響:探究H?是否在炎癥期(傷口后1-3天)加速M1向M2轉化。
區分作用機制:對比H?與抗氧化劑NAC的效果,明確H?是否依賴抗氧化途徑。
闡明細胞來源:確認外周血單核細胞是否為H?誘導的M2巨噬細胞來源。
研究思路
動物模型建立:
構建小鼠背部全層皮膚缺損模型(圖1C),分為H?吸入組、NAC處理組和對照組。
H?組每日吸入66%H?+33%O?混合氣2小時(圖1A-B)。
時間序列分析:
在傷口后24、48、72小時取樣,檢測炎癥細胞浸潤(H&E染色)、巨噬細胞極化(免疫熒光)、血清細胞因子(ELISA)及轉錄組變化。
體外驗證:
使用THP-1細胞模擬巨噬細胞極化,H?飽和培養基處理(圖3E-F)。
機制排除:
通過Unisense微電極確認H?處理組與對照組培養基氧含量一致,排除氧濃度干擾(方法4.5)。
關鍵數據及其研究意義
H?減少炎癥細胞浸潤(圖1E,圖2)
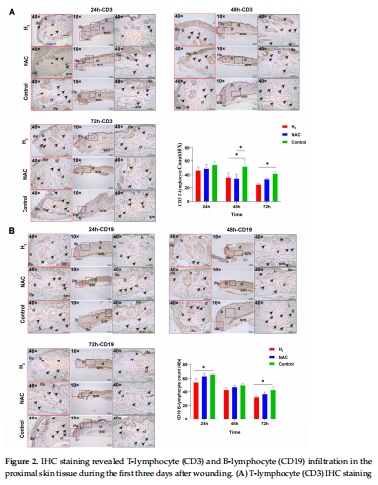
數據:H&E和IHC染色顯示,H?組傷口近端組織在72小時內炎癥細胞(T/B淋巴細胞)浸潤顯著低于對照組(p<0.05)。
意義:證實H?早期抑制炎癥反應,為后續巨噬細胞極化研究奠定基礎。
H?提前誘導M2巨噬細胞極化(圖3)
數據:
免疫熒光:H?組第3天M2巨噬細胞比例達70%(對照組<40%),M2/M1比值顯著升高(圖3B-C)。
qRT-PCR:M2標志基因(CD163)表達上調(p<0.05)(圖3D)。
意義:首次揭示H?在傷口后第3天(而非常規第5-7天)完成M1向M2轉化,加速炎癥消退。
轉錄組與細胞因子譜驗證(圖4-5)
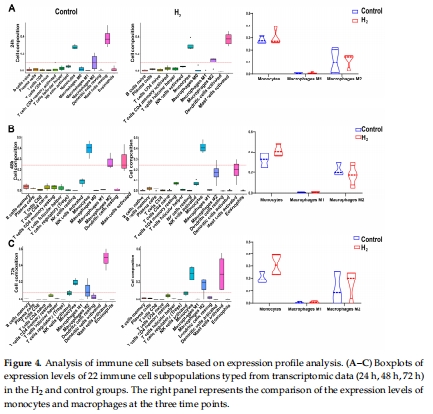
數據:
CIBERSORT分析:H?組單核細胞增多,M2巨噬細胞比例升高(圖4C)。
血清因子:H?組第3天促炎因子(IFN-γ、IL-6)下降,抗炎因子IL-10升高(圖5F)。
意義:多維度證實H?通過調節免疫細胞分布和細胞因子平衡促進抗炎微環境。
H?作用超越抗氧化機制(圖3F)
數據:H?組M2極化效果顯著優于NAC組(p<0.05),且NAC組M2比例滯后。
意義:H?的促愈合機制不依賴ROS清除,可能涉及直接調控巨噬細胞表型轉換。
結論
核心發現:H?通過誘導早期(傷口后第3天)M2巨噬細胞極化,縮短炎癥期,加速傷口愈合。
機制創新:H?的作用獨立于抗氧化途徑,可能通過調節單核細胞募集和極化相關基因(如STAT6、TGF-β)實現。
臨床價值:為慢性難愈性傷口(如糖尿病足潰瘍)提供新型氣體治療策略。
丹麥Unisense微電極的應用意義
技術原理與實驗設計
測量原理:Unisense微電極基于電化學還原反應(H?→2H?+2e?),實時檢測溶解H?濃度(μM級精度)。
實驗場景:用于驗證H?飽和培養基的溶解H?濃度(方法4.5),確保體外實驗中H?處理組與對照組氧含量一致(排除氧干擾)。
關鍵研究意義
排除混雜因素:
證實H?處理未改變培養基氧分壓,避免氧濃度差異對巨噬細胞極化的潛在影響(如缺氧誘導M2極化)。
為“H?直接調控極化”的結論提供關鍵支撐(圖3F)。
量化H?遞送效率:
精確測定溶解H?濃度,確保體外實驗與體內吸入治療的H?生物可利用度一致性。
技術優勢:
高靈敏度:可檢測低至nM級H?濃度,適用于細胞微環境監測。
實時動態:秒級分辨率捕捉H?擴散動力學,優于傳統氣相色譜等終點檢測。
局限性與拓展方向
空間分辨率限制:單點測量難以反映組織內H?梯度分布(如傷口中心與邊緣)。
未來應用:結合活體成像技術,可實時監測傷口局部H?濃度與巨噬細胞表型的時空關聯。
總結
Unisense微電極在本研究中作為質量控制工具,通過精準量化溶解H?濃度,排除了氧分壓對實驗結果的干擾,為“H?直接誘導M2極化”的機制結論提供了不可替代的技術支持。其高靈敏度和實時性優勢,為氣體分子(H?、CO等)在免疫調控研究中的應用樹立了嚴謹的方法學標準。