熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
標(biāo)題:Unimolecular Self-Assembled Hemicyanine-Oleic Acid Conjugate Acts as a Novel Succinate Dehydrogenase Inhibitor to Amplify Photodynamic Therapy and Eliminate Cancer Stem Cells
單分子自組裝半菁-油酸偶聯(lián)物作為一種新型琥珀酸脫氫酶抑制劑,可放大光動(dòng)力療法
期刊:Wang et al. 2023
摘要內(nèi)容
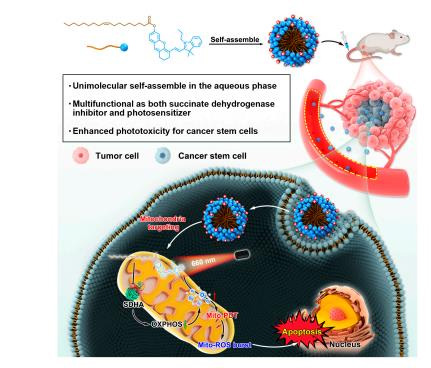
本研究開發(fā)了一種新型線粒體靶向的自組裝納米顆粒(CyOA NPs),由血青素-油酸共軛物(hemicyanine-oleic acid conjugate)構(gòu)成,無需外源輔料即可自組裝成超分子納米顆粒。CyOA NPs具有雙重功能:
抑制氧化磷酸化(OXPHOS):靶向線粒體復(fù)合物II的琥珀酸脫氫酶(SDHA),降低氧氣消耗,逆轉(zhuǎn)腫瘤缺氧;
增強(qiáng)光動(dòng)力療法(PDT):在660 nm激光照射下產(chǎn)生線粒體活性氧(Mito-ROS),顯著殺傷乳腺癌干細(xì)胞(BCSCs)。
在4T1乳腺癌模型和BCSC模型中,CyOA NPs的抑瘤效果和抗轉(zhuǎn)移能力均優(yōu)于臨床光敏劑Hiporfin,且無顯著毒性。
研究目的
解決傳統(tǒng)光動(dòng)力療法(PDT)的固有瓶頸:
活性氧(ROS)壽命短、擴(kuò)散距離有限;
實(shí)體瘤缺氧環(huán)境限制PDT療效;
癌癥干細(xì)胞(CSCs)對(duì)常規(guī)治療的耐藥性。
研究思路
分子設(shè)計(jì):
將油酸(oleic acid)與血青素染料(IR780/IR783衍生物)共軛,合成 CyOA 和 SO?-CyOA(圖2A)。
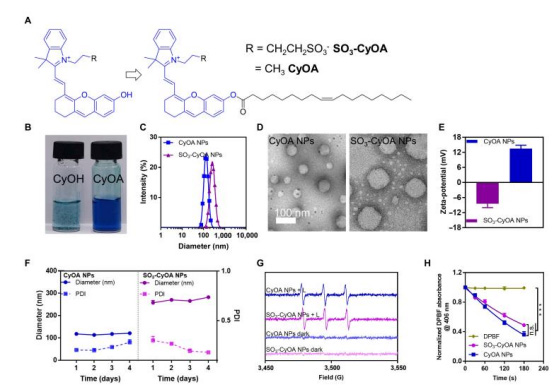
利用油酸的疏水性驅(qū)動(dòng)自組裝形成納米顆粒(CyOA NPs/SO?-CyOA NPs)。
機(jī)制驗(yàn)證:
缺氧逆轉(zhuǎn):證實(shí)CyOA靶向SDHA抑制OXPHOS,降低氧氣消耗(圖3C-E);
線粒體靶向PDT:CyOA NPs富集于線粒體,激光照射后產(chǎn)生高濃度Mito-ROS(圖4B)。
療效評(píng)估:
體外:比較CyOA NPs與SO?-CyOA NPs對(duì)BCSCs的殺傷效果(圖4C-E);
體內(nèi):在4T1和BCSC移植瘤模型中評(píng)估抑瘤及抗轉(zhuǎn)移能力(圖5)。
測量數(shù)據(jù)及研究意義
缺氧緩解與OXPHOS抑制(圖3)
數(shù)據(jù):
Clark電極顯示CyOA NPs處理組細(xì)胞耗氧率降低40%(圖3C);
Seahorse分析表明CyOA抑制基礎(chǔ)/最大呼吸速率(圖3D);
ATP合成減少(圖3E),Hif-1α表達(dá)下調(diào)(圖3F)。
意義:首次發(fā)現(xiàn)CyOA直接結(jié)合SDHA(分子對(duì)接與免疫共沉淀驗(yàn)證,圖3G-H),逆轉(zhuǎn)腫瘤缺氧,為PDT提供內(nèi)源性氧氣支持。
ROS生成與細(xì)胞殺傷(圖4)
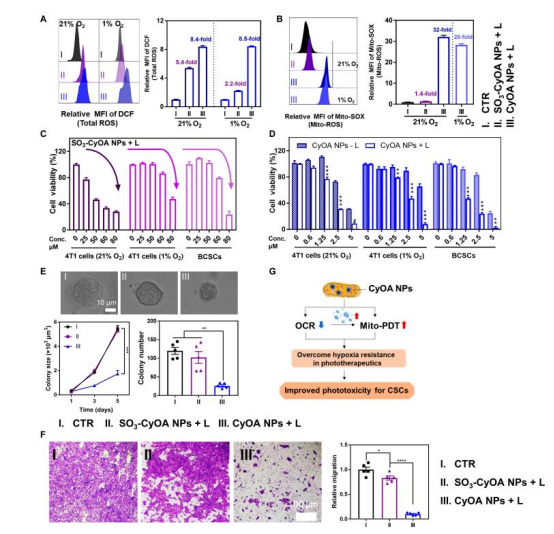
數(shù)據(jù):
流式細(xì)胞術(shù)顯示CyOA NPs在缺氧下仍產(chǎn)生高水平Mito-ROS(32倍于對(duì)照組,圖4B);
對(duì)BCSCs的IC??為1.4 μM(SO?-CyOA NPs為70.6 μM),抑制乳腺球形成(圖4C-E)。
意義:缺氧耐受性PDT高效殺傷CSCs,克服傳統(tǒng)PDT瓶頸。
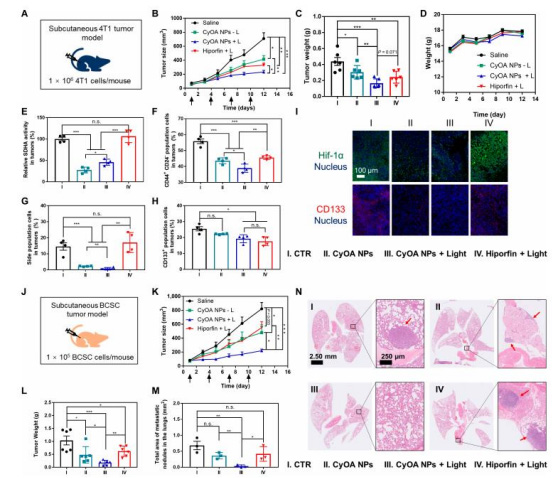
體內(nèi)抗腫瘤效果(圖5)
數(shù)據(jù):
CyOA NPs+L組在4T1模型中抑瘤率67%(Hiporfin組53%),肺轉(zhuǎn)移結(jié)節(jié)減少(圖5B-C, M-N);
BCSC模型中抑瘤率83%(圖5L),CD44?CD24? CSC比例下降62%(圖5F)。
意義:自組裝納米顆粒兼具靶向遞送、缺氧調(diào)節(jié)與PDT功能,顯著抑制腫瘤生長和轉(zhuǎn)移。
丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
測量方法(Materials and Methods)
使用Unisense Clark氧電極直接監(jiān)測細(xì)胞培養(yǎng)液中溶解氧濃度變化(圖3C)。
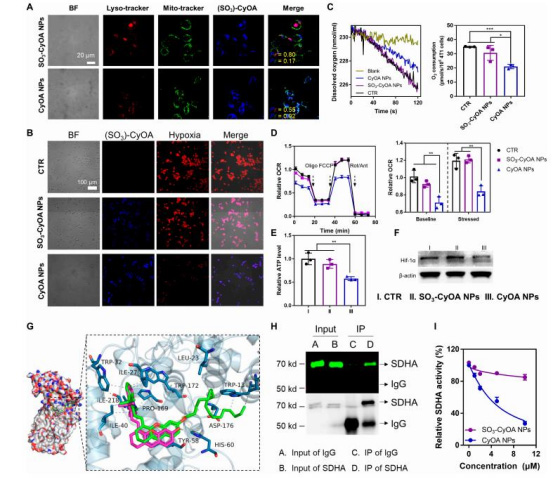
研究意義:
直接量化OXPHOS抑制:通過實(shí)時(shí)記錄氧氣消耗速率,證明CyOA NPs顯著降低細(xì)胞呼吸作用(40%降幅),為"氧氣節(jié)約"策略提供直接證據(jù)。
技術(shù)優(yōu)勢:相較于間接檢測(如Hif-1α表達(dá)),Clark電極提供動(dòng)態(tài)、高靈敏度的氧氣代謝數(shù)據(jù),與Seahorse分析互補(bǔ),共同驗(yàn)證CyOA的OXPHOS抑制機(jī)制。
生理相關(guān)性:在近似生理?xiàng)l件下(37°C,密閉系統(tǒng))測量,數(shù)據(jù)更貼近體內(nèi)微環(huán)境,支持CyOA在實(shí)體瘤缺氧調(diào)控中的轉(zhuǎn)化價(jià)值。
結(jié)論
雙重功能分子設(shè)計(jì):CyOA NPs是首個(gè)兼具SDHA抑制劑和線粒體靶向光敏劑的自組裝納米顆粒,通過抑制OXPHOS逆轉(zhuǎn)腫瘤缺氧,并增強(qiáng)PDT。
高效清除CSCs:對(duì)BCSCs的光毒性比SO?-CyOA NPs高50.4倍,顯著抑制乳腺球形成和腫瘤遷移。
臨床轉(zhuǎn)化潛力:在移植瘤模型中療效優(yōu)于臨床光敏劑Hiporfin,且無系統(tǒng)性毒性(圖5),為克服PDT耐藥性提供新策略。