熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Intestine-Targeted Controlled Hydrogen-Releasing MgH2 Microcapsules for Improving the Mitochondrial Metabolism of Inflammatory Bowel Disease
用于改善炎癥性腸病線粒體代謝的腸道靶向控釋氫化鎂微膠囊
來源:Adv. Funct. Mater. 2024, 34, 2316227
先進功能材料
摘要內容:
該研究開發了一種新型腸道靶向控釋氫化鎂微膠囊(MgH?@EC@ES),通過多層乳化法將MgH?微粒包封于乙基纖維素(EC)疏水網絡內,外層覆以Eudragit S100(ES)。該微膠囊在胃酸環境中穩定,在腸道pH響應下溶脹并持續水解釋放氫氣(H?)。在結腸炎小鼠模型中,高劑量口服該微膠囊的預防效果與一線藥物5-氨基水楊酸(5-ASA)相當(體重/脾臟重量和疾病活動性改善),且在結腸長度恢復和組織病理學改善方面優于5-ASA。機制上,H?通過保護線粒體電子傳遞鏈(ETC)復合體免受氧化損傷,增強腸細胞能量代謝,促進黏膜修復。
研究目的:
解決炎癥性腸病(IBD)治療中高效低毒藥物的需求,克服傳統氫氣療法(如富氫水)載氫量低、胃酸分解導致腸道氫氣生物利用度不足的問題,實現腸道靶向、高劑量、持續性的氫氣遞送。
研究思路:
材料設計與合成:
采用多步乳化法構建核殼結構微膠囊(MgH?@EC@ES):
核心:MgH?微粒嵌入疏水性乙基纖維素(EC)網絡,延緩水解。
外殼:pH響應型Eudragit S100(ES),胃部(pH 1.2)不溶,腸道(pH 7.0)溶脹允許水分滲透。
體外性能驗證:
表征微膠囊形貌、結構(SEM、共聚焦顯微鏡)。
測試模擬胃腸液中的穩定性及pH響應釋氫行為(GC、氫電極)。
體內遞送與分布:
熒光/Cy5標記追蹤微膠囊在胃腸道的轉運(活體成像)。
氫電極直接測量結腸局部H?濃度。
療效與機制研究:
DSS誘導結腸炎小鼠模型,評估微膠囊預防效果(體重、DAI、結腸長度、組織病理)。
對比5-ASA和MgSO?@EC@ES(無H?釋放對照)。
通過轉錄組測序、ATP檢測、線粒體復合體蛋白分析等揭示H?保護線粒體ETC、增強能量代謝的機制。
測量數據及其研究意義(標注圖表來源):
材料表征:
SEM(圖1c, g)和共聚焦成像(圖1f):確認微膠囊核殼結構及MgH?均勻分散,意義:驗證合成策略成功實現MgH?的包封與保護。
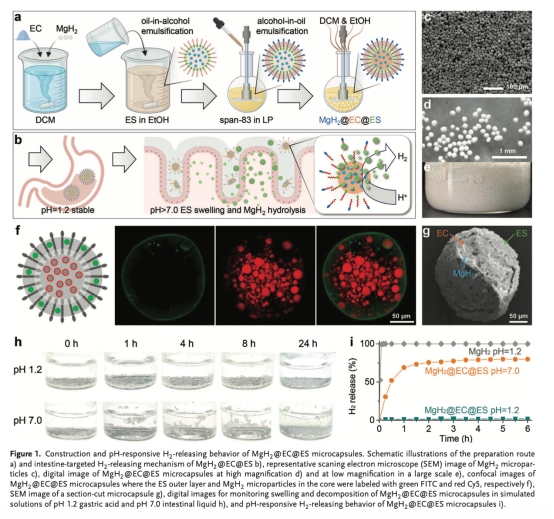
XRD、FTIR:證明包封過程未破壞MgH?晶體結構,成分符合設計。
體外釋氫行為:
模擬胃液(pH 1.2)中微膠囊形態穩定且無H?釋放(圖1h);模擬腸液(pH 7.0)中持續釋氫>48小時(圖1i,)。意義:證實pH響應靶向釋氫特性,避免胃部分解。
體內分布與氫氣生物利用度:
熒光成像(圖2a-c如下)和ICP測鎂含量:微膠囊口服后4-6小時主要富集于腸道,12小時后逐漸排出。
Unisense氫電極測量結腸H?濃度(圖2d 如下):
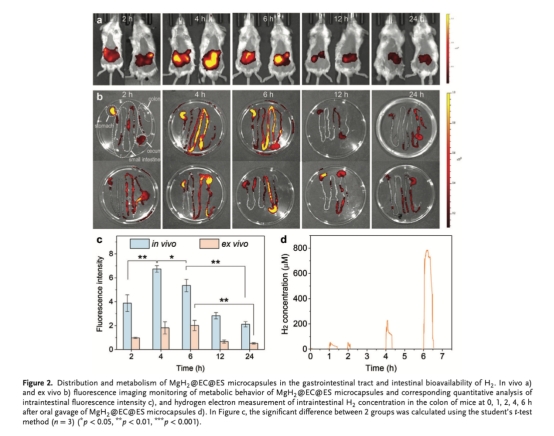
數據:給藥后4小時結腸H?濃度顯著上升,6小時達飽和溶解度(約0.8 mM)。
研究意義:直接證明微膠囊在目標部位(結腸)實現了高濃度、持續性的H?遞送,解決了口服MgH?粉末或富氫水在腸道H?生物利用度低的關鍵問題。該數據是驗證"腸道靶向高效遞氫"核心假設的直接證據。
治療效果數據:
體重變化、DAI評分(圖3b-c 如下):高劑量微膠囊(800 mg/kg)效果與5-ASA相當,顯著優于模型組。
結腸長度恢復(圖3d, f)、脾臟重量減小(圖3d, g)、組織病理評分改善(圖3e, h):微膠囊效果優于5-ASA,且依賴H?釋放(MgSO?@EC@ES無效)。意義:證實微膠囊的優越治療效能。
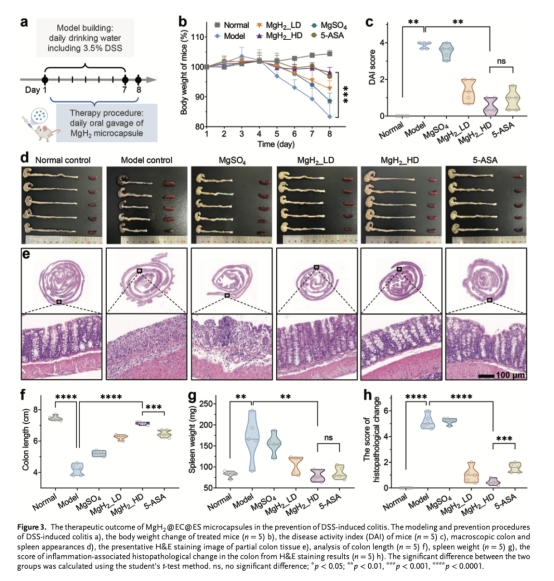
腸道屏障修復(圖4):微膠囊上調緊密連接蛋白(ZO-1, Occludin)表達,促進腸上皮細胞增殖(Ki-67)和類器官生長(圖4g-h),意義:揭示H?促進黏膜修復的細胞機制。
分子機制數據:

轉錄組測序(圖5):富集到線粒體相關基因和氧化磷酸化通路上調。
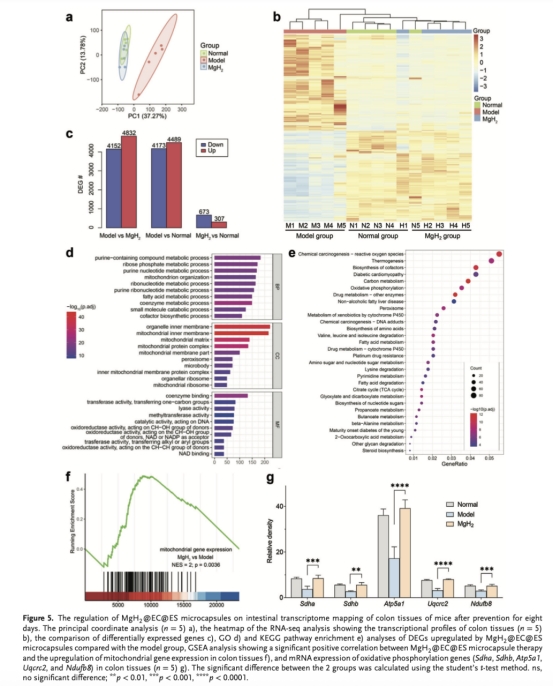
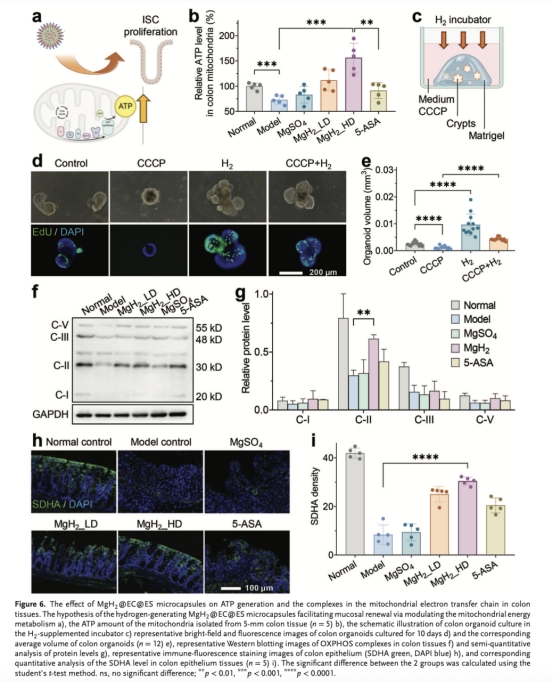
ATP水平檢測(圖6b如下):微膠囊顯著恢復結腸線粒體ATP產量。
線粒體ETC復合體蛋白水平(圖6f-g, i):H?特異性保護復合體II(SDHA)等免受氧化損傷。意義:創新性揭示H?通過維護ETC功能增強能量代謝,支持黏膜修復。
結論:
成功開發具有核殼結構的腸道靶向控釋MgH?微膠囊(MgH?@EC@ES),實現口服后結腸局部高濃度、持續性H?釋放。
高劑量微膠囊在結腸炎預防中綜合療效優于一線藥物5-ASA,尤其在促進黏膜修復(結腸長度恢復、組織病理改善)方面。
機制上首次揭示:H?通過靶向保護線粒體ETC復合體(尤其是復合體II)免受氧化損傷,增強腸細胞能量代謝,從而促進上皮再生和屏障修復。該研究為氫氣療法在IBD中的應用提供了創新劑型和機制見解。
丹麥Unisense電極測量數據的詳細解讀:
使用Unisense微電極在小鼠結腸腔內直接測量的溶解H?濃度數據(圖2d)具有以下關鍵研究意義:
靶向遞送驗證:給藥后前2小時結腸H?濃度極低,證明微膠囊在胃部(酸性環境)幾乎不釋氫;4-6小時濃度驟升并達飽和,明確證實微膠囊僅在腸道環境響應性釋氫,實現精準靶向。
生物利用度量化:6小時結腸H?濃度達0.8 mM(生理飽和濃度),遠高于富氫水的遞送能力(通常<0.8 mM且持續時間短),解決了傳統氫氣療法腸道劑量不足的瓶頸。
藥效相關性:H?濃度峰值時間(4-6小時)與微膠囊腸道滯留峰值(圖2c)及最佳治療效果時段吻合,為"高劑量腸道H?直接驅動療效"提供直接證據。
技術優勢:相較于間接檢測(如血液H?濃度),原位電極測量更準確反映結腸局部生物可利用H?水平,是評價腸道靶向遞送系統的金標準。